
ОБЪЕДИНЕНИЕ КОМБУСТИОЛОГОВ
«МИР БЕЗ ОЖОГОВ»
ГИПЕРОСМОЛЯНЫЙ СИНДРОМ У ОБОЖЖЕННЫХ
Ушакова Т.А.
Ожоговый центр, ФГБУ Институт хирургии им.А.В.Вишневского МЗ РФ,
Кафедра термических поражений, ран и раневой инфекции ГБОУ ДПО РМАПО МЗ РФ, Москва.
АКТУАЛЬНОСТЬ. Нарушения водно-электролитного баланса – общемедицинская проблема. В отделениях интенсивной терапии эти нарушения наблюдаются у 10% пациентов, при этом, чаще — у больных в критических состояниях (1). Показано влияние гипернатриемии на летальность у пациентов с черепно-мозговой травмой (2), подтвержден риск фатального исхода в случае развития гипернатриемии при тяжелом диабете (3). При ожогах свыше 30% п.т. практически всегда развивается отечный синдром (4). На основе ряда исследований было сделано предположение о том, что баланс жидкости и электролитов сложно регулировать, в том числе, из-за недостатка соответствующих знаний и опыта у лечащих врачей, что, в свою очередь, влияет на увеличение частоты осложнений и летальных исходов, особенно среди хирургических больных (5).
ЦЕЛЬ. Обосновать необходимость соблюдения принципов патогенетического подхода в диагностике и лечении тяжелообожженных пациентов с гиперосмолярным синдромом.
ВВЕДЕНИЕ. Известно, что вода в организме составляет примерно 60% массы тела и распределяется в двух основных пространствах: внутриклеточном и внеклеточном, функционально отделенных клеточной мембраной. Последняя за счет натриевого насоса поддерживает натрий во внеклеточном секторе в виде его главного осмотического компонента, в то время калий удерживается в качестве внутриклеточного катиона. При тяжелой патологии «выкачивание» натрия из клетки нарушается и он накапливается в ней, приводя к синдрому «больной клетки» (5).
Внеклеточное пространство подразделяется на внутрисосудистый и внесосудистый (в основном, интерстиций) компартменты, разделенные полупроницаемой мембраной, свободно проницаемой только для воды, направление движения которой подчинено законам осмоса. Осмотическое давление или осмоляльность раствора определяется количеством осмотически активных частиц, растворенных в объеме растворителя. К последним относятся электролиты и неэлектролиты, белок. Осмоляльность плазмы – жесткая, как и pH, константа и составляет 275-295 мосмоль/кг воды, осмолярность – концентрационный показатель — мосмоль/л воды. В случае с организмом это одна и та же величина. Осмолярность можно рассчитать по формуле известных концентраций: 2(Na+К) + [глюкоза] + [мочевина] + 0,03[белок] (6). Эффективную осмоляльность раствора называют тоничностью. При повышении осмоляльности экстрацеллюлярной жидкости до 320 – 330 мосмоль/кг наступают явные клинические симптомы со стороны ЦНС, связанные с обезвоживанием клеток мозга. При осмоляльности 360 – 380 мосмоль/кг развивается кома. Гиперосмолярный синдром обусловлен, в основном, гипернатриемией (1, 5-8).
РЕГУЛЯЦИЯ. В норме пусковым сигналом к ответной реакции на водно-солевой дисбаланс является жажда. В организме имеются центральные (в гипоталамусе) и периферические (воротная вена, почки и др. органы) осморецепторы. Однако, у пациентов в критическом состоянии в силу их тяжести и проводимой им интенсивной терапии этот главный симптом «размыт» (9).
Регуляция ВСО – сложный механизм взаимодействия нейро-гуморальных факторов, направленных на поддержание гомеостаза в организме. Практически все гормоны участвуют в этом процессе. Однако, наиболее значимыми в рамках обсуждаемой темы, являются вазопрессин (старое название антидиуретического гормона) и альдостерон.
Вазопрессин – первичный регулятор осмолярности плазмы — образуется в ядрах гипоталамуса и поступает в кровь из нейрогипофиза. Действует посредством активации трех типов рецепторов: 1) V1α или V1 – вызывают вазоконстрикцию; 2) гипофизарные V1β или V3–участвуют в секреции АКТГ; 3) почечные V2– снижают экскрецию воды (10).
Почки – орган, в котором происходит основная реализация нейро-гормональной регуляции водно-солевого баланса. Именно через V2 рецепторы на поверхности базолатеральной мембраны эпителия дистальных канальцев и в большей степени собирательных трубок вазопрессин осуществляет активную реабсорбцию воды. Несомненно, только в здоровой нормально функционирующей почке возможен энергозависимый внутриклеточный каскад биохимических реакций, включающий экспрессию рецепторов, образование цАМФ, который пересекает клетку и активирует протеинкиназы, фосфорилирование мембранных белков, повышающих проницаемость мебраны для воды. В результате ультраструктурной перестройки в клетке образуются вакуоли для переноса больших потоков воды по осмотическому градиенту от апикальной к базолатеральной мембране, не позволяя самой клетке набухать. Кроме того, в дистальых канальцах вазопрессин активирует выход из клеток гиалуронидаз, расщепляющих межклеточное вещество, что способствует пассивному транспорту воды по осмотическому градиенту (7) .
Альдостерон – известный минералокортикоид, оказывающий многообразное влияние на водно-солевой обмен: 1) усиливает реабсорбцию натрия в проксимальных отделах нефрона; 2) усиливает экскрецию калия и протона; 3) стимулирует выведение натрия из клетки и захват ими калия. Сосудистые эффекты симпатической нервной системы (изменения кровотока почки при критических состояниях) вызывают активацию ренин-ангиотензинальдостероновой системы (5). Кроме того, в ответ на стрессорное истощение глюкокортикоидной фракции минералокортикоиды частично выполняют их функцию, в связи с чем у такого рода пациентов может развиться синдром вторичного гиперальдостеронизма (6).
В последние годы открыта и продолжает изучаться роль натрийуретических пептидов в регуляции ВСО. Это целое семейство пептидов – гормонов, секретируемых предсердием, желудочком и эндотелиальными клетками сосудов при их растяжении и гипернатриемии. В мозге, сосудах, почках, надпочечниках и легких выделены рецепторы для натрийуретических пептидов — А, В и С (11). Функции этих пептидов схожи: ингибирование реабсорбции натрия в проксимальных почечных канальцах и секреции ренина и альдостерона. В настоящее время наиболее стабильным в диагностическом плане признан предшественник «мозгового» натрийуретического пептида — NT-proBNP. Продемонстрирована корреляция его повышения при сердечной и почечной патологии (11-13). Имеются неопубликованные данные о диагностической значимости NT-proBNP при системной интерстициальной отечности.
Колоссальную роль в регуляции обмена между внутрисосудистым и внесосудистым секторами, особенно патогенетически значимое у пациентов, которым проводится инфузионная терапия, имеют гидростатическое и коллоидно-осмотическое давления (КОД) – факторы Старлинга. Гидростатическое давление в капиллярах (обеспечение которого – осмолярность плазмы) обуславливает диффузию жидкости в интерстиций, КОД – движение жидкости из интерстиция. В норме размеры пор мембран клеток эндотелия капилляров ограничивают выход белка из плазмы, обеспечивая в ней более высокое онкотическое давление, чем в интерстиции. Однако даже у здоровых людей общий внутрисосудистый альбумин проходит через интерстициальное пространство один раз каждые 24-48 часов. Воспалительные цитокины увеличивают диаметр пор в месте повреждения, что приводит к локальному отеку. В случае тяжелого заболевания, травмы, ожогов развивается генерализованная реакция увеличения капиллярной проницаемости, следствием чего является массивный выход плазмы в интерстиций и снижение ОЦК (5). Движение плазмы усиливается в связи с гиперосмолярностью обожженной поверхности, что приводит к еще большей эндотелиальной проницаемости и диффузии в интерстиций белка, в основном альбумина, обладающего способностью удерживать воду массой, в 17 раз превышающую его собственную. Высокое коллоидно-осмотическое давление интерстиция приводит к задержке жидкости в межклеточном пространстве, ликвидация которой требует значительных лечебных усилий в отличие от других отёков, которые регрессируют по достижении компенсации основного заболевания [4].
Продолжается исследование патогенеза гиперосмолярного синдрома на молекулярном уровне. Выявлено, что гиперосмолярный синдром снижает экспрессию медиатора провоспалительного ответа –TNF-α (14), а изоформы гидратированного натрия оказывают патологическое влияние на клетки, в частности, на кардиомиоциты (15).
В ответ на гиперосмолярное содержимое трахеобронхиального дерева, связанное с испарением воды при обструктивной астме, в клетках эпителия синтезируется релаксирующий фактор (EpDRF), способствующий бронходилатации (16,17). Осмотическая резистентность клеточных мембран снижается при хронических заболеваниях. Появились данные о восстановлении осмотической резистентности эритроцитов после хирургического лечения эмфиземы (18).
КЛАССИФИКАЦИЯ, ЭТИОЛОГИЯ. Основными формами проявления нарушений водно-электролитного баланса являются гипо- и гипернатриемия. Каждое из электролитных расстройств может развиться при гипо-, нормо- или гиперволемии. Гипонатриемия ([Na] < 135 ммоль/л) в ситуации гиповолемиии наблюдается, например, при циррозе печени, гиперволемии – при повреждении миокарда и нормоволемии – при синдроме несоответствия секреции АДГ (19). Первичный избыток электролита (натрия) влечет за собой вторичный избыток воды. Некоторые авторы считают, однако, что первичны расстройства водного баланса, а электролитные проявления вторичны (20). На наш взгляд, это верно лишь отчасти. В условиях интенсивной терапии электролитные нарушения могут быть ятрогенны (1,10). Среди основных причин гипернатриемии ([Na] > 145 ммоль/л) у пациентов в критических состояниях называется избыточное введение растворов натрия (1,6,8). Высокообъемные инфузии, как известно, используют при лечении гиповолемического шока при ожогах, кровотечениях (4,21). Имеет значение и проводимая фармакологическая терапия, которая может оказывать влияние на различные регуляторные звенья ВСО. Например, растворы глюкозы, превышающие ее пороговую концентрацию и вызывающие осмотический диурез.
В целом, гипернатриемия развивается при двух состояниях: увеличения поступления натрия или дефицита воды. К первой группе причин, как уже сказано, относятся: 1) избыточное введение растворов натрия и 2) первичный или вторичный гиперальдостеронизм (1,4,6).
Уменьшение общей воды – наиболее частая причина гипернатриемии. Среди способствующих этому состоянию факторов отмечают: 1) ятрогенные: избыточное применение сальуретиков и осмотического диуреза; 2) потери воды в клетку; 3) плазмопотеря при ожоговом шоке и испарение воды с раны; 4) интестинальные и легочные потери; 5) почечная (тубулярная) недостаточность; 6) секвестрация жидкости в «третье пространство» и т.д. (1,6,8).
В связи со сложными причинно-следственными связями водно-электролитного дисбаланса и подчас его «неклассическим» проявлением диагностика и лечение нарушений ВСО могут быть затруднительны.
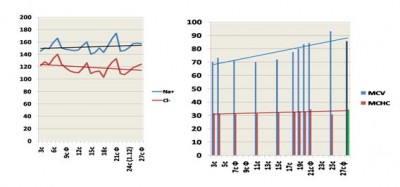
Рис 1. Гиперосмолярный синдром у б.З. (ожоги 80% п.т., УГДФ 7 сут)
Классический послешоковый гиперосмолярный синдром у тяжелообожженной пациентки З. (рис.1) вызвавший значительное уменьшение объема эритроцитов (сморщивание). Интенсивная терапия с применением ультрагемодиафильтрации (УГДФ) способствовала периодической нормализации концентраций электролитов. Однако, нарушения мембранной проницаемости прогрессировали, что привело к необратимому внутриклеточному отеку.
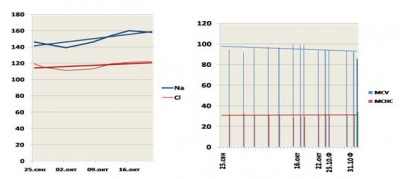
Рис 2. Гиперосмолярный синдром у б.Т. (ожоги 60%п.т., УГДФ 4 сут)
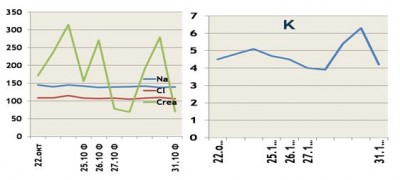
Рис 3. Проявления почечной недостаточности у б.Т. (ожоги 60%п.т., УГДФ 4 сут)
Умеренно выраженный хронический гиперосмолярный синдром с «неклассическим» увеличением объема эритроцитов наблюдали у б.Т. (рис.2), что свидетельствует о возможных первичных нарушениях водного баланса, приведших к значительному нарушению мембранной проницаемости и току жидкости внутрь клеток. Через месяц на этом фоне у пациента манифестировалась почечная недостаточность, успешно корригируемая интенсивной терапией с применением УГДФ (рис.3).
Для своевременной и адекватной диагностики и лечения водно-электролитных нарушений предлагаем следующие рекомендации.
РЕКОМЕНДАЦИИ.
А. Мониторинг. Диагностический алгоритм водно-электролитных нарушений у тяжелообожженных пациентов в условиях интенсивной терапии должен включать регулярный комплекс клинико-лабораторных исследований, на основании которого врач может получать максимально возможную информацию для мониторирования ответа организма на проводимые мероприятия с целью квалифицированной коррекции и профилактики усугубления водно-электролитных сдвигов.
Диагностический мониторинг водно-электролитных нарушений:
I. Лабораторная диагностика
1) Na, K, Cl, Glu, Crea, NT-proBNP, осмолярность плазмы;
2) Клинический анализ крови: Hb, Ht, MCV, MCHC;
3) Биохимия крови: общий белок, альбумин, мочевина, креатинин;
4) Осмоляльность мочи, суточные: электролиты, мочевина, креатинин, глюкоза;
5) Коллоидно-осмотическое давление (КОД) плазмы крови.
II. Клиническое обследование: динамика веса, ЦВД, наличие отеков в «третье пространство».
III. Тщательная детализация в/в инфузий: объем, качественные характеристики (кристаллоиды или коллоиды, тоничность).
IV. Анализ выбора диуретиков для повышения экскреции калия, натрия или осмотического диуреза;
V. Анализ фармтерапии — выявление препаратов, влияющих на АДГ, на [Na] (например, карбенициллин);
VI. Необходимо также учитывать особенности патогенеза ожогового шока. Быстрая и высокообъемная коррекция гиповолемического шока (плазмопотеря → изоосмолярная дегидратация) в зависимости от свойств инфузионных растворов может привести в последующем к различным нарушениям ВСО: 1) гипоосмолярной гиперволемии (общая гипергидратация, гемодилюция), 2) гиперосмолярной гиперволемии (↑введение Nа, жидкости), 3) гиперосмолярной гиповолемии (↓воды вследствие применения осмотического диуреза).
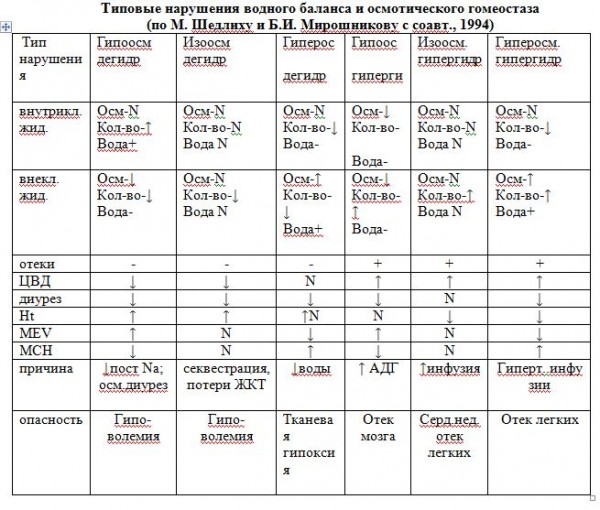
Неоценимую помощь в диагностике водно-электролитного дисбаланса могут оказать разработанные схемы типовых нарушений (6), подобно представленной в сокращенном варианте (табл.1).
Табл.1
Б. Коррекция. Основные рекомендации по коррекции гипо- и гипернатриемии сводятся к расчету дефицита воды и электролитов, темпу и длительности введения инфузионных растворов и мониторингу. Различают острые и хронические нарушения ВСО: в случае сохранения водно-электролитного дисбаланса более суток говорят о хроническом состоянии (1).
Несомненно, ликвидация водного дисбаланса, восполнение жидкости и (или) электролитов являются первоочередной задачей. При этом необходимо соблюдать общие принципы лечения нарушений ВСО: 1) производить расчет дефицита воды по формуле: % теоретического содержания воды в организме х текущий вес пациента х ([Na] в плазме крови/ норма [Na] – 1); 2) при острых состояниях коррекцию можно проводить в течение суток, при хронических – 2-3 суток, стараясь снизить гипернатриемию за сутки не более, чем на 10 ммолль/л; 3) оценить дефицит электролитов по формуле: 0,2 х вес больного х (норма-истинная [C] электролита); 4) устранить жизненно-опасные нарушения; 5) вводить в первые сутки – ½ всего расчетного объема; 6) проводить мониторинг [Na] каждые 4-8 час в течение 1-х суток (1).
Особенно важно соблюдать постепенный темп в лечении гипонатриемии – более тяжелого синдрома, связанного с ментальным расстройством, обусловленным отеком мозга (1, 19, 20, 22). Специфическая терапия при гипонатриемии включает гипервентиляцию, введение гиперосмолярных веществ (3% раствор NaCl), глюкокортикоидов (снижают отечность мозга), антагониста вазопрессина ваптана (19, 22-24), при сопутствующей гипергидратации — гемофильтрацию (8). При гипернатриемии используют гипотоничные растворы (0,45% раствор NaCl), фуросемид (снижает тубулярную реабсорбцию натрия), спиронолактон (конкурентный антагонист альдостерона), ведутся исследования по применению предсердного натрийуретического фактора (25, 26), малых доз вазопрессина (27).
ОБСУЖДЕНИЕ.
Диагностика и лечение нарушений ВСО – комплексная задача. При сохранении гиперосмолярного синдрома, несмотря на устранение ятрогенных причин его развития, необходимо проводить срочный диагностический поиск «скрытых» потерь воды в интерстиций, клетки, серозные полости, третье пространство. В противном случае однозначные методы элиминации натрия путем дальнейшей гипергидратации и осмотического диуреза, тем более, ультрагемодиафильтрации, могут привести к утяжелению синдрома «больных клеток» вплоть до их гибели. Клинической манифестацией в таком случае будет полиорганная недостаточность.
Крайне важными с профилактической целью могут быть стандартные правила: удерживать коллоидно-осмотическое давление плазмы крови, улучшать реологию периферии, не допускать водные перегрузки, стабилизировать проницаемость эндотелия.
ВЫВОДЫ. В патогенезе ожоговой болезни и, в первую очередь, ожогового шока, ключевую роль играют водно-электролитные нарушения, коррекция которых возможна только при тщательном клинико-диагностическом мониторинге.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
- http://www.uptodate.com/contents
- Kolmodin L, Sekhon MS, Henderson WR, Turgeon AF, Griesdale DE. Hypernatremia in patients with severe traumatic brain injury: a systematic review// Ann Intensive Care. — 2013 Nov 6; 3(1):35.
- Maggiore U, Picetti E, Antonucci E, Parenti E, Regolisti G, Mergoni M, Vezzani A, Cabassi A, Fiaccadori E. The relation between the incidence of hypernatremia and mortality in patients with severe traumatic brain injury //Crit Care. — 2009; 13(4):R110.
- Фисталь Э.Я., Сперанский И.И., Самойленко Г.Е., Арефьев В.В. Патогенез, классификация, диагностика и лечение отёчного синдрома у обожжённых //Комбустиология, электронная версия. — N 34 / 2008.
- L. Sobotka, S. P. Allisson и Z. Stanga. Вода и электролиты //http://www.critical.ru/
- Зайчик А.Ш., Чурилов Л.П. Основы общей патологии. Часть 2. Основы патохимии/ СПб., ЭЛБИ, — 2000,-688с.
- http://doctor-v.ru/
- Мима М. Горн, Урсула И. Хейтц, Памела Л. Сверинген. Водно-электролитный и кислотно-основной баланс./ Пер. с англ. — СПб.-М.: «Невский Диалект»- «Издательство БИНОМ», 2000.-320с.
- Shoshana Arai, RN, PhD, Assistant adjunct professor in physiological nursing, Nancy Stotts, RN, EdD, and Kathleen Puntillo, RN, DNSc. Thirst in Critically Ill Patients: From Physiology to Sensation// Am J Crit Care. — 2013 July; 22(4): 328–335.
- Vantyghem MC, Balavoine AS, Wémeau JL, Douillard C. Hyponatremia and antidiuresis syndrome//Ann Endocrinol (Paris). — 2011 Dec;72(6):500-12.
- http://www.medee.ru/laboratory-research/
- www.ncbi.nlm.nih.gov/pubmed/20023254
- Fu S, Luo L, Ye P, Yi S, Liu Y, Zhu B, Wang L, Xiao T, Bai Y. The ability of NT-proBNP to detect chronic heart failure and predict all-cause mortality is higher in elderly Chinese coronary artery disease patients with chronic kidney disease// J. Clinical Interventions in Aging.- April 2013 Volume 2013:8 Pages 409 – 417.
- Banerjee A, Moore EE, McLaughlin NJ, Lee L, Jones WL, Johnson JL, Nydam TL, Silliman CC. Hyperosmolarity attenuates TNF-α-mediated proinflammatory activation of human pulmonary microvascular endothelial cells// Shock. — 2013 Apr;39(4):366-72.
- Madonna R, De Caterina R. Sodium-hydrogen exchangers (NHE) in human cardiovascular diseases: Interfering strategies and their therapeutic applications //Vascul Pharmacol. — 2013 Oct 15.
- Fedan JS, Thompson JA, Ismailoglu UB, Jing Y. Tracheal epithelium cell volume responses to hyperosmolar, isosmolar and hypoosmolar solutions: relation to epithelium-derived relaxing factor (EpDRF) effects//Front Physiol. — 2013 Oct 11;4:287.
- Jing Y, Dowdy JA, Van Scott MR, Fedan JS. Hyperosmolarity-induced dilation and epithelial bioelectric responses of guinea pig trachea in vitro: role of kinase signaling//J Pharmacol Exp Ther. — 2008 Jul; 326(1):186-95.
- Mineo TC, Sellitri F, Tacconi F, Ambrogi V, Tamburrini A, Mineo D. Erythrocyte osmotic resistance recovery after lung volume reduction surgery//Eur J Cardiothorac Surg. — 2013 Sep 25.
- Palm C, Wagner A, Gross P. [Hypo- and hypernatremia]//Dtsch Med Wochenschr. — 2011 Jan;136(1-2):29-33.
- Agrawal V, Agarwal M, Joshi SR, Ghosh AK. Hyponatremia and hypernatremia: disorders of water balance// J Assoc Physicians India. — 2008 Dec;56:956-64.
- Hultström M. Neurohormonal interactions on the renal oxygen delivery and consumption in haemorrhagic shock-induced acute kidney injury. //Acta Physiol (Oxf). — 2013 Jul 10.
- Dietrich W, Erbguth F. [Increased intracranial pressure and brain edema]. Med Klin Intensivmed Notfmed. — 2013 Mar;108 (2):157-69.
- Srinivasan S, Benneyworth B, Garton HJ, Hervey-Jumper SL, Raimer PL, Odetola FO, Han YY. Intracranial pressure/cerebral perfusion pressure-targeted management of life-threatening intracranial hypertension complicating diabetic ketoacidosis-associated cerebral edema: a case report//Pediatr Emerg Care. — 2012 Jul;28(7):696-8.
- Decourcey DD, Steil GM, Wypij D, Agus MS. Increasing use of hypertonic saline over mannitol in the treatment of symptomatic cerebral edema in pediatric diabetic ketoacidosis: an 11-year retrospective analysis of mortality*. -Pediatr Crit Care Med. 2013 Sep;14(7):694-700.
- Swärd K, Valsson F, Sellgren J, Ricksten SE. Differential effects of human atrial natriuretic peptide and furosemide on glomerular filtration rate and renal oxygen consumption in humans// Intensive Care Med. — 2005 Jan;31(1):79-85.
- Redfors B, Bragadottir G, Sellgren J, Swärd K, Ricksten SE. Dopamine increases renal oxygenation: a clinical study in post-cardiac surgery patients//Acta Anaesthesiol Scand. — 2010 Feb;54(2):183-90.
- Bragadottir G, Redfors B, Nygren A, Sellgren J, Ricksten SE. Low-dose vasopressin increases glomerular filtration rate, but impairs renal oxygenation in post-cardiac surgery patients// Acta Anaesthesiol Scand. — 2009 Sep;53(8):1052-9.