
ОБЪЕДИНЕНИЕ КОМБУСТИОЛОГОВ
«МИР БЕЗ ОЖОГОВ»
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПОСТРАДАВШИХ ОТ ОЖОГОВ (ОБЗОР ЛИТЕРАТУРЫ)
Плешков А.С., Шаповалов С.Г., Панов А.В.
ФГБУ ВЦЭРМ им. А.М. Никифорова МЧС России, Санкт-Петербург
Хирургическое лечение является одной из актуальных проблем комбустиологии [14, 15, 44]. Как любая мультидисциплинарная задача, лечение обожжённых, должно представлять собой симфонию взаимодействия анестезиологии и реаниматологии, клинической фармакологии, лабораторной диагностики, тканевой инженерии, медицинской психологии, нутрициологии и многих других специальностей. Однако первой скрипкой, определяющей тактику и прогноз лечения пострадавшего, остаётся хирургия, и в перспективе, её значение будет только увеличиваться.
С позиции своего скромного клинического опыта, авторы не претендуют на формирование методических рекомендаций. Целью данного обзора скорее является привлечение внимания к наиболее, на взгляд авторов, проблемным вопросам хирургии ожогов.
Под термином хирургическое лечение подразумевается спектр выполняемых при ожогах оперативных вмешательств. Туалет ран, бескровный химический некролиз, смена повязок не могут быть отнесены к данной категории, как не обладающие существенными признаками хирургической операции: разъединением и соединением жизнеспособных тканей, наличием значительной травмы [3]. Внесение этих манипуляций в перечень операций, возможно, и приносит экономический эффект в противостоянии со страховыми компаниями, но тормозит развитие комбустиологии, маскируя низкую хирургическую активность, формируя отношение к операции, как к рутинной безопасной манипуляции, не требующей особых навыков и подготовки [6].
Не все ожоговые раны являются объектом хирургического лечения. Лечение поверхностных ожогов, поражающих эпидермис и верхние слои дермы, является консервативным и, обычно, не представляет особых сложностей. Использование современных атравматичных перевязочных материалов, тщательный контроль инфекции в ране позволяют добиться заживления в сроки не более двух недель [3, 42].
Сложнее обстоит дело с, так называемыми, «пограничными» и «мозаичными» ожогами, поражающими глубокие слои дермы. Формирование ожогового струпа и частые неудовлетворительные исходы консервативного лечения приближают данную группу в плане выбора лечебной тактики к глубоким ожогам. При этом хирург, трезво оценивая риски и негативные последствия операции, должен принять решение о необходимости хирургического лечения в каждом конкретном случае [21, 37, 49]. Значительные изменения в тактику лечения пограничных ожогов, по-видимому, принесут активно внедряемые препараты для ферментативного очищения ран: NexoBrid, Debrase [45, 46]. Это новое поколение высокоэффективных средств позволяет в течение нескольких часов добиться селективного очищения от нежизнеспособных тканей и определить потенциал раны к спонтанному заживлению. К сожалению, отечественное здравоохранение пока не располагает опытом их применения.
Безусловным показанием для хирургического лечения является наличие у пострадавшего глубоких ожогов. В дальнейшем, мы будем иметь в виду только эту группу пациентов. Традиционно выделяют три группы оперативных вмешательств, выполняемых при ожогах: декомпрессионные операции, некрэктомии и операции по восстановлению кожного покрова.
Декомпрессионные операции – некротомии и фасциотомии выполняются в ранние сроки в экстренном порядке при циркулярных ожогах конечностей и туловища, а также при тяжёлых электроожогах. Показания и техника выполнения этих вмешательств хорошо известны и не требуют подробного обсуждения [4, 11].
Основой хирургического лечения глубоких ожогов являются иссечение погибших тканей и оперативное восстановление кожного покрова.
Сроки начала хирургического лечения имеют большое значение для дальнейшего течения ожоговой болезни, определения прогноза пострадавшего, и служили предметом дискуссии в 70-80-е годы XX века. Тема раннего или превентивного хирургического лечения ожогов является одной из «вечно молодых». Изменение взглядов на хирургическую тактику никак нельзя считать достижением последних десятилетий [8]. Ещё в 1966 году в своём фундаментальном труде «Термические поражения» патриарх отечественной комбустиологии Т.Я. Арьев писал: «A priori несомненно, что чем раньше будут иссечены омертвевшие ткани ожоговой раны и чем скорее будет пластически замещён операционный дефект, образовавшийся в результате этого иссечения, тем меньшая вероятность различных осложнений ожогов и в тем более короткие сроки наступит излечение. Уточняя приоритет раннего производства операций при ожогах, Stör (1952) указывал, что 27 апреля 1935 года на заседании научно-медицинского общества в Кёнигсберге Läwen демонстрировал больную, которой он иссёк ожоговую рану на руке и заместил образовавшийся дефект по Тиршу. Вихриев Б.М., отмечая работу Läwen, назвал и ряд других авторов, произведших аналогичные казуистические операции задолго до него (Wilms, 1901; Sczypiorsky, 1903 и др.)». Далее автор приводит опыт работы собственной клиники до и после введения раннего хирургического лечения в 1961 году (sic!) с явным улучшением исходов [3].
Несмотря на вышеизложенное, наибольшее распространение в нашей стране получила концепция консервативной подготовки ран к аутодермопластике к 3-4 неделе после ожога. Формального отказа от иссечения струпа в ранние сроки не провозглашалось [4, 8], однако показания к нему были определены весьма узкие, что на практике привело к почти полному отказу от ранних некрэктомий в пользу высушивания струпа [14]. Свою роль сыграл и перманентный дефицит качественных раневых покрытий и препаратов крови [11].
Альтернативный вариант, получивший распространение в США к 70-м годам ХХ века усилиями Janzekovic, Heimbach, Herndon, предусматривал, как можно более раннее иссечение поражённых тканей с одномоментным замещением дефекта расщеплённой кожей [27, 29, 31]. Такой подход требовал высокой квалификации персонала, наличия специального оснащения, больших запасов препаратов крови. Являясь более ресурсо- и энергозатратным, раннее хирургическое лечение ожогов обеспечивает не только сокращение сроков госпитализации, но и, как показывает практика, снижение летальности, улучшение функциональных и эстетических результатов лечения [9, 30, 32].
Необходимость раннего удаления ожогового струпа основывается на его роли в патофизиологии термической травмы. Очаг первичного некроза, возникающий непосредственно в момент ожога, представляет собой значительный источник токсических веществ, которые при резорбции имеют негативные патофизиологические эффекты, как на локальный статус в области раны, так и на общее состояние пострадавшего [3, 4]. В зоне первичного некроза и окружающей её зоне стаза, со сниженным уровнем метаболизма клеток, создаются благоприятные условия для роста патогенных микроорганизмов [11]. Бактериальная колонизация струпа может привести не только к углублению раны, путём лизиса окружающих здоровых тканей, но и к развитию системной инфекции – одного из наиболее серьёзных осложнений ожогов [37]. Подобные резорбтивные эффекты, колонизация струпа патогенными микроорганизмами и гнойное воспаление, как начало процессов демаркации, обычно разворачиваются на 5-7 сутки после травмы. Таким образом, оптимальными сроками иссечения ожогового струпа являются первые 3-4 дня после травмы.
При обширных глубоких ожогах (более 10% поверхности тела), требующих многоэтапного иссечения, нужно стремиться, чтобы этот срок не превышал 10 суток [37, 49]. Приступать к хирургическому лечению тяжелообожженных обычно рекомендуется по выходу из ожогового шока [11, 39, 49]. Вмешательства на фоне нестабильной гемодинамики и серьёзных нарушений периферического кровообращения представляют собой малооправданный риск [11]. При обширных глубоких ожогах площадь хирургические некрэктомии за один этап следует планировать исходя из 1/2 – 1/3 площади глубокого поражения. Большинство авторов сходятся на иссечении 10-15% поверхности тела в качестве максимального объёма операции [11, 37, 49]. Сверхагрессивного иссечения участков с неустановленной глубиной поражения нужно избегать [44]. Активная хирургическая тактика достоверно повышает сроки выживаемости и снижает летальность в группе пациентов с критическими ожогами [13, 14, 16, 19, 27, 29, 30, 50].
Некрэктомия преследует цель перевести ожоговую рану, характеризующуюся массивом фиксированных коагуляционных некрозов, в равномерно кровоточащую, чистую хирургическую рану. По замечанию Т.Я.Арьева, по своей сути она эквивалентна первичной хирургической обработке в общей хирургии [3]. Дополнительной целью ранней некрэктомии является предотвращение формирования патологических грануляций в зоне демаркации, так как именно они считаются ответственными за формирование впоследствии патологических рубцов [44]. В своих обзорах Devis и Deitch убедительно продемонстрировали, что заживление ожоговой раны дольше 21 дня повышает риск формирования гипертрофических рубцов до 80%. Более того, они показали, что раннее оперативное восстановление кожного покрова снижает вероятность формирования патологических рубцов, по сравнению с отсроченной пластикой [21, 22].
Нередки ситуации, когда пациент поступает в специализированное ожоговое отделение через значительный период после получения травмы, когда оптимальные сроки для выполнения первичной некрэктомии уже упущены. Риск оперативного вмешательства возрастает: в условиях развившегося острого воспаления возможно увеличение кровопотери [11, 14, 48], повышается вероятность септических осложнений [3, 11]. Во многих работах указывалось на неудовлетворительные результаты одномоментных аутодермопластик после поздних некрэктомий [4, 14].
Взвесив эти риски, мы призываем не отказываться от выполнения некрэктомии, так как она является патогенетическим лечением по своему характеру. Особенностями выполнения операции в данных условиях будут: повышенное внимание к гемостазу, отказ от одномоментной аутодермопластики, широкое использование антисептиков и раневых покрытий с антибактериальными свойствами. В некоторых случаях может потребоваться консервативная предоперационная подготовка, направленная на высушивание колликвационных некрозов и купирование местных признаков воспаления.
В проекте клинических рекомендаций «Хирургическое лечение пострадавших от ожогов» предлагается следующая классификация хирургических некрэктомий:
- первичная хирургическая некрэктомия – выполняемая до развития в ране клинических признаков воспаления;
- отсроченная хирургическая некрэктомия – выполняемую на фоне воспалительной реакции;
- этапная хирургическая некрэктомия – выполняемую в несколько программируемых этапов, не на всей площади при обширных зонах глубокого поражения;
- вторичная хирургическая некрэктомия – выполняемую при возникновении вторичных и третичных некрозов в зонах первичной или отсроченной некрэктомии.
По технике выполнения выделяют:
- тангенциальную некрэктомию – послойное иссечение нежизнеспособных тканей с помощью дерматома или некротомов;
- иссечение единым блоком, при котором выполняется радикальное удаление струпа в пределах здоровых тканей.
Некоторые авторы дополнительно выделяют дермабразию – щадящее механическое удаление омертвевшего эпидермиса и поверхностных слоёв дермы с помощью фрезы или других инструментов для обеспечения оптимального спонтанного заживления пограничных ожогов [21, 37].
Тангенциальное иссечение позволяет добиться впоследствии лучших эстетических и функциональных результатов, однако приводит к большей кровопотере и не всегда обеспечивает радикальность [37, 44].
Иссечение единым блоком требует удаления значительного массива изначально жизнеспособных тканей, приводит к формированию выраженного дефекта в зоне операции, но даёт более надёжный результат и обычно сопровождается меньшей кровопотерей [14, 49].
Частным видом хирургической некрэктомии является ампутация или дезартикуляция пораженной конечности или ее сегмента. Безусловно, возможно комбинированное применение разных техник иссечения струпа у одного пациента.
Выполнение тангенциальной некрэктомии с помощью ножей Humby и Weck обеспечивает быстрое и максимально прецизионное удаление погибших тканей, позволяет сохранить систему подкожных вен, обеспечивает хорошие отдалённые функциональные и эстетические результаты. Необходимая глубина иссечения определяется по равномерности кровоточивости тканей (по этой причине избегают инфильтрации иссекаемой зоны растворами вазоконстрикторов). Объем кровопотери при тангенциальной некрэктомии обычно не превышает 0,75 мл на квадратный сантиметр иссечения и восполняется по показаниям в послеоперационном периоде [14, 48]. Для сокращения кровопотери рекомендуется:
- создание предоперационной гемодилюции,
- использование пневможгутов для иссечений на конечностях,
- аппликационное применение раствора адреналина для достижения гемостаза в ране,
- интраоперационные трансфузии свежезамороженной плазмы,
- использование раневых покрытий с гемостатическими свойствами (такими, по нашему мнению, являются препараты на основе алло- и ксенокожи),
- наложение давящих или эластичных бинтов в качестве фиксирующей послеоперационной повязки.
Важным является подержание нормальной температуры тела пациента во время вмешательства. Операция обычно осуществляется в очень тёплом помещении (+25…+27°С), хирургические поля изолируются, чтобы снизить потери через испарение или радиацию. Рекомендуется выполнение комплекса мероприятий по предотвращению гипотермии: использование согревающих одеял, источников инфракрасного излучения, устройств для согревания инфузионных растворов и воздуха в дыхательных контурах [44, 49].
Идеальным вариантом окончания некрэктомии является выполнение одномоментной аутодермопластики. Однако это вмешательство всегда сопряжено с риском потери трансплантатов, так как в настоящее время отсутствуют доступные и достоверные способы определения границ некроза [44, 49].
Объективное определение зоны некроза в ранние сроки невозможно ещё и по той причине, что её граница имеет свойство смещаться в зону стаза до 4-5 суток в зависимости от общего состояния больного и адекватности проводимой терапии [3, 11, 25, 44].
Следует учитывать, что результаты одномоментных пластик у тяжелообожжённых достоверно хуже, чем при ограниченных ожогах. В масштабном исследовании Gore D. и соавторов в 2001г. было показано, что у пациентов с ожогами около 60% п.т. средний процент приживления аутодермотрансплантатов составил 88%, по сравнению с 95% в контрольной группе с ограниченными ожогами [24].
Как правило, частота выполнения одномоментных аутодермопластик составляет около 30%. Обычно это пациенты с ограниченными ожогами, без подозрения на субфасциальное поражение.
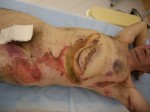
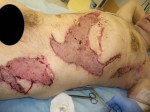
Рис.1 Результат первичной некрэктомии с одномоментной аутодермопластикой.
В других случаях операцию заканчивают наложением временных раневых покрытий – заменителей кожных покровов. Требования, предъявляемые к этим раневым покрытиям исключительно высоки [11, 49]. Прежде всего, они должны обладать барьерной функцией, присущей здоровой коже, т.е. предотвращать потерю тепла, влаги и электролитов, а также препятствовать проникновению микроорганизмов. Весьма желательно наличие у временных покрытий антибактериальных и гемостатических свойств. Они должны быть достаточно пластичны для выполнения сложного рельефа иссечённой раны и надёжно фиксироваться к ней. Пренебрежение этими требованиями приводит к высыханию раны, вторичному инфицированию и, в итоге, нивелирует результаты операции.
Традиционно временные покрытия подразделяются на продукты биологического происхождения и синтетические. «Золотым стандартом» считается свежая человеческая донорская (чаще трупная) кожа – аллотрансплантат (по устаревшей классификации гомотрансплантат) [12, 23, 49].
Несмотря на то, что использование донорской кожи при лечении ожогов во всём мире активно практикуется ещё с 50-х годов ХХ века [49], в нашей стране к настоящему времени этот ценный лечебный ресурс практически недоступен.
Бурное развитие клеточных технологий и тканевой инженерии в последние десятиления XX века привело к появлению целого ряда полусинтетических продуктов на основе материалов биологического происхождения пригодных для временного закрытия иссечённых ожоговых ран [17, 43, 49].
В распоряжении отечественных хирургов имеются препараты ксеногенного происхождения (ксено- или по старой классификации гетеротрансплантаты): донорская кожа животных, чаще свиней. Свиная кожа может применяться в виде свежего трансплантата. В этом варианте она обладает высокими лечебными свойствами, но несёт риск передачи зоонозов (бруцеллёз, сибирская язва и другие), а также риск инфицирования условно патогенной флорой. Кроме того, процесс согласования с источником (животноводческим предприятием), заготовка, экспресс-определение биологической безопасности, доставка в операционную делают её применение на срочной операции, которой является первичная некрэктомия, трудноразрешимой задачей. По этой причине широкое распространение получили препараты лиофилизированной свиной кожи (Ксенодерм). Они стерильно упакованы, биологически безопасны и готовы к применению. Сохраняющее структуру, но не содержащее живых клеток покрытие, естественно уступает по лечебным свойствам жизнеспособной коже, но служит компромиссом между доступностью, безопасностью и эффектом. Покрытие хорошо моделируется по поверхности раны, обладает адгезией и удовлетворительной барьерной функцией. Клинически отмечается наличие у него гемостатических свойств. Обычно, мы покрываем его вторичной гидрофобной мазевой повязкой, чтобы избежать преждевременного высыхания.
Из опыта применения широкого спектра синтетических раневых покрытий заслуживает внимания использование двухслойных полупроницаемых полиуретановых пластин (Epigard, Suspur-derm). При надёжной фиксации к дну раны они обеспечивают хорошую барьерную функцию, стимулируют рост грануляционной ткани. Следует отметить, что под покрытиями нередко образуются гематомы, а их механические свойства не позволяют обеспечить плотное прилегание в сложных анатомических зонах. В целом, на наш взгляд, для временного закрытия обширных ран, губчатые раневые покрытия обладают преимуществами перед другими группами повязок, такими как гидрогели, порошки и плёнки.
При отсутствии раневых покрытий допустимым представляется использование многослойных марлевых повязок с мазями на жирорастворимой основе [6].
Оптимальный момент для отсроченного восстановления кожного покрова после тангенциальной некрэктомии, помимо состояния больного, определяется свойствами повязки. Покрытия биологического происхождения способны удовлетворительно функционировать 5-7 дней и более, для синтетических покрытий этот период обычно ограничивается 2-3 сутками. Раневое ложе, которое сохранило жизнеспособность под временным покрытием к этому сроку, является пригодным для пересадки аутокожи. Хорошим критерием готовности реципиентного ложа является начало роста грануляционной ткани [37].
Восстановление кожного покрова, как уже упоминалось, является ключевой задачей хирургического лечения ожогов. Т.Я. Арьев по этому поводу писал: «В 1939г., когда был изобретён дерматом, окончилась многовековая предыстория лечения ожогов и началась его подлинная история. Объективный опыт учит, что именно этот метод впервые действительно позволил снизить летальность от ожогов» [3]. Аутодермопластика с помощью дерматомов различных конструкций давно стала рутинной операцией в отделениях, специализирующихся на лечении ожоговой травмы [4, 11]. Технические особенности её выполнения хорошо знакомы каждому комбустиологу. Возможно использование как расщеплённых, так и полнослойных кожных трансплантатов. При планировании операции необходимо помнить, что расщепленный трансплантат подвергается выраженной контракции после приживления, а полнослойный – сокращается сразу после забора, но затем практически не ретрагирует. Считается, что расщеплённые трансплантаты приживают лучше, чем полнослойные. Это связано с тем, что в первые дни после пересадки питание кожи осуществляется за счёт осмоса, и более тонкий слой клеток с открытой капиллярной сетью получает лучшее питание [11].
При большой площади поражения, требующей многоэтапных операций, критическое значение имеет последовательность восстановления кожного покрова в различных анатомических зонах. Современная тактика предусматривает приоритет восстановления кожи для обеспечения сосудистого доступа и трахеостомии (периклавикулярные области, шея, паховые области). Восстановление кожи на функционально и эстетически значимых областях можно перенести на второй этап, когда сформировалась достоверная картина глубины поражения, и ниже риск вторичных некрозов [44]. Кроме того, предваряющий хирургию, этап консервативного лечения ожоговых ран может снижать общую потребность в пересадке кожи у некоторых пациентов [28, 42]. Раннее восстановление кожного покрова областей крупных суставов и кистей важно с точки зрения раннего начала реабилитации, так как отсутствие функции на фоне гиперкатаболизма быстро приводит к неизбежному поражению опорно-двигательного аппарата и формированию контрактур [44].
Особого подхода заслуживает лечение глубоких ожогов лица. Большинство хирургов, путём консервативного лечения, стараются сохранить так много местных специфичных тканей, насколько это возможно [28, 49]. Хирургическая некрэктомия обычно выполняется отсрочено. Однако существуют авторитетные сторонники и агрессивной тактики, такие как Klein и Engrav [20]. Они пропагандируют ранее иссечение в пределах, так называемых, эстетических зон, в случае если имеются глубокие поражения более 80% их поверхности. В ситуации отсроченного восстановления кожного покрова в качестве временного покрытия оптимально использование аллокожи.
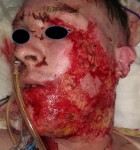
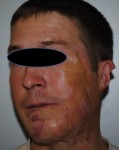
Рис.2 Результат некрэктомии и аутодермопластики на лице.
Ещё одним принципиальным моментом мы считаем обязательное прогнозирование и оценку результатов аутодермопластики. Приживление менее 60% трансплантата в настоящее время нельзя признать приемлемым исходом операции. Скрупулёзный анализ результатов и причин неудач аутодермопластик является важным путём к улучшению исходов лечения [6].
Одной из наиболее серьёзных задач, которую приходится решать хирургу при лечении тяжелообожжённых, является дефицит донорских ресурсов для восстановления кожного покрова. Проблема возникает при площади глубокого поражения свыше 30-40% поверхности тела [11, 36]. Максимальную площадь утраченного кожного покрова, которая может быть восстановлена, определяют возможности методов экономной пластики:
- использование сетчатых перфорированных трансплантатов (Lanz, 1908),
- MEEK-техника (Meek, 1958),
- микроаутодермопластика.
Ключевым понятием для экономных методов пересадки кожи является коэффициент пластики (КП) – отношение площади исходного аутодермотрансплантата к площади участка ран, закрытого сеткой или марками полученными из этого трансплантата [11].
Использование сетчатых трансплантатов, без преувеличения, совершило революцию в оказании помощи обожжённым [11, 49]. С помощью перфораторов можно быстро получить трансплантаты имеющие коэффициент пластики 1:1,5, 1:2, 1:3, 1:4. Последнее отношение оценивается, как предел метода для достижения спонтанной эпителизации в ячейках [11]. Впрочем, имеются модели перфораторов с коэффициентом 1:6 и более. Современные модели перфораторов позволяют получать любой из перечисленных коэффициентов на одном аппарате с помощью замены пластины-подложки для трансплантата.
В последние годы было обращено внимание на несоответствие между заявленным производителем и фактическим коэффициентом пластики для сетчатых трансплантатов. По данным Kamolz L.P., опросившем 40 врачей-комбустиологов из разных центров Европы и США, наиболее часто употребляемый коэффициент пластики 1:3 (используют 82% хирургов) обеспечивает реальный коэффициент лишь 1:1,6, а 1:1,5 – 1,3 [36].
Альтернативой сетчатым трансплантатам, предложенной ещё в 1958 году, является Meek-техника [33, 40]. Её применение требует особого оснащения и расходных материалов, однако, базируется на несложном принципе [16]. Трансплантаты накладываются на пробковые подложки квадратной формы и дважды разрезаются во взаимно перпендикулярных направлениях на квадратики со стороной 2 мм (рис.3).
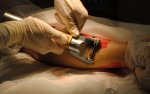


Рис.3 Этапы аутодермопластики по методике MEEK.
Для облегчения нанесения на раны квадратики наклеиваются на особые тканевые носители с заданным коэффициентом растяжения 1:3, 1:4, 1:6 или 1:9 (рис.4).


Рис.4 Этапы аутодермопластики по методике MEEK.
На этих носителях микротрансплантаты фиксируются на ранах до 5-х суток. После приживления ткань удаляется, и раны ведутся по общим принципам, обеспечивающим активную краевую эпителизацию (рис.5).
а. 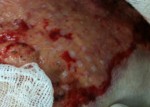 б.
б. 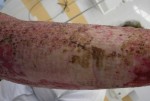
Рис.5 Этапы аутодермопластики по методике MEEK.
а- на 5-е сутки после операции, после удаления тканевого носителя; б- на 12-е сутки после операции.
Спонтанная эпителизация ран в промежутках между микротрансплантатами достигается при коэффициенте пластики 1:6. Методика значительно более трудоёмкая, требует специального оборудования и увеличения операционной бригады. Преимуществом является то, что достигаемый коэффициент пластики точно соответствует заявленному производителем, что продемонстрировано на снимке (рис.6):

Рис.6 Сравнение коэффициента пластики 1:3 для сетчатого трансплантата и методики Meek.
Другим преимуществом метода является возможность использования даже мелких кусочков кожи, тогда как для получения сетчатого трансплантата подходит только значительный по размерам, забранный без дефектов, фрагмент кожи.
Оригинальная модификация метода микроаутодермопластики была описана в 1986 году китайскими хирургами [11, 35, 52]. Расщеплённую кожу накладывали на бумагу и разрезали на полоски шириной 1 мм, а затем нарезали на мелкие кусочки. Полученные микротрансплантаты помещались в ванночки с физиологическим раствором. Кусочки кожи всплывали эпидермальной стороной вверх. Раствор из ванночки сливали, на микротрансплантаты накладывали кусок шёлковой ткани и с его помощью переносили их на раневые поверхности. Последующие исследования показали, что даже неправильно ориентированные кусочки кожи вносят свой вклад в эпителизацию [11]. Сверху микротрансплантаты закрывали аллодермотрансплантатами. Наличие донорской кожи играет важную роль, поскольку наблюдается постепенное замещение структур аллодермы аутологичными тканями. С менее надёжным эффектом возможно использование и других временных раневых покрытий. Авторами был достигнут коэффициент пластики 1:10,5, а в эксперименте на животных и 1:30 [35]. Метод, несмотря на свою высокую эффективность, чрезвычайно трудоёмкий и, судя по представленным авторами исходам, часто даёт неудовлетворительные функциональные и эстетические результаты.
Несомненно, что различные виды микроаутодермопластики являются одним из путей для восстановления кожного покрова при обширных ожогах. При этом стандартом, на настоящий момент, остаётся метод аутодермопластики с использованием перфорированных сетчатых трансплантатов.
Однако лечение пациентов с глубокими поражениями более 30% п.т. представляет для хирурга трудноразрешимую задачу, поскольку донорские ресурсы оказываются крайне ограниченными. Решением вопроса дефицита донорских ресурсов могло бы быть широкое использование аутологичных биотехнологических эквивалентов кожи [11, 37]. В тоже время, даже в развитых странах западной Европы, эти продукты не вошли в рутинную практику. Используемые с начала 80-х годов прошлого века методика лечения с использованием аутологичных кератиноцитов (CEA – cultured epidermal autografts: Rheinwald J.G., Green H., 1977.) характеризуются длительным сроком культивировирования, составляющим 2-3 недели, невысокой жизнеспособностью, будучи перенесёнными на иссечённую рану, при изолированном применении дают неприемлемый функциональный и эстетический результат, и кроме того, чрезвычайно дороги [47, 51]. Перспективные достижения регенеративной медицины и тканевой инженерии обеспечат настоящий прорыв в области лечения пострадавших с критическими ожогами.
Особую группу в плане хирургического лечения составляют пациенты с ограниченными ожогами, вовлекающими глубокие анатомические структуры: кости, мышцы, сухожилия. Украинскими коллегами предложен термин «субфасциальные» поражения [5]. Такие поражения могут быть вызваны, например, высоковольтным электричеством, или контактом с высокотемпературным агентом. Раневые дефекты у этой группы пострадавших, после выполнения некрэктомии, обычно требуют замещения не просто кожей, а тканевыми комплексами. Выполнение таких операций должно осуществляться в соответствии с правилами пластической хирургии.
С точки зрения реконструктивной пластической хирургии выделяется три категории нарушений покровных тканей [38]:
- рана,
- дефект,
- деформация.
Под раной понимается разрушение тканей. Примером может служить открытый перелом. Для раны устранения необходимы идентификация и соединение всех повреждённых частей.
Дефект – потеря тканей. Восстановление дефекта требует переноса тканей из других областей.
Деформация – неправильное взаиморасположение тканей. Примером деформации может служить послеожоговая рубцовая контрактура, для устранения которой требуется перемещение местных тканей.
Несомненно, что проблема у индивидуального пациента чаще представлена сочетанием различных категорий. Значение выделения этих категорий демонстрируется неправильной реконструктивной тактикой: бесперспективно устранять дефект попыткой стягивания краёв или нанесения послабляющих разрезов. Выбор необходимого метода реконструкции при этом может определяться так называемой «реконструктивной лестницей» [38].
Ступень 1: заживление вторичным натяжением.
Ступень 2: наложение швов и заживление первичным натяжением.
Ступень 3: отсроченное затягивание швов или острое растяжение местных тканей.
Ступень 4: пластика расщеплённым кожным трансплантатом.
Ступень 5: пластика полнослойным кожным трансплантатом.
Ступень 6: хроническое растяжение местных тканей (экспандерная дермотензия).
Ступень 7: пластика местными лоскутами с рандомизированным кровоснабжением.
Ступень 8: пластика местными лоскутами с осевым кровоснабжением.
Ступень 9: свободная пересадка комплексов тканей (лоскутов) с наложением микрохирургических анастомозов.
Последовательно двигаясь по «ступеням» этой лестницы, хирург оценивает возможности каждого метода для устранения конкретной проблемы. Наиболее простой метод (близкий к основанию лестницы), является самым надёжным, и расценивается, как метод выбора. Правило не является жёсткой догмой, но хорошим подспорьем в выборе оптимального пути реконструкции.
Исходя из вышеизложенного, понятно, что ожоги с вовлечением глубоких анатомических структур приводят к формированию сложного по составу дефекта. Следовательно, для его устранения рекомендуются методы, обеспечивающие локальное создание или перенос комплекса тканей: ступени 6-9. Простой пересадки кожи недостаточно, поскольку дефект охватывает и более глубокие структуры: жировую клетчатку, фасцию, мышцы, кость. Широкое распространение получили: метод экспандерной дермотензии для лечения глубоких ожогов волосистой части головы, а также применение пахового лоскута для лечения глубоких ожогов кисти (рис.7).
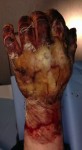
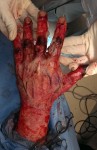
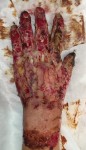
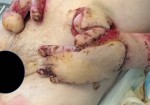
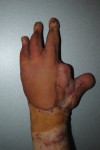
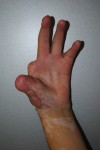
Рис.7 Применение пахового лоскута для закрытия дефекта кисти.
а-при поступлении на 5-е сутки после травмы; б- выполнение тангенциальной некрэктомии; в- результат одномоментной аутодермопластики; г- двухсторонняя пластика паховыми лоскутами (с ампутацией 2 пальца левой кисти); д,е- результат пластики.
Хорошо известны работы отечественных хирургов по применению лопаточного и торакодорзального лоскутов в свободном и несвободном вариантах [1, 7].
Таким образом, хирургическое лечение ожогов является актуальной проблемой, требующей продуманного решения. При этом ведущее значение имеет доступность расходных материалов: раневых покрытий, перевязочных средств, одноразовых лезвий, препаратов крови и т.д. Однозначно, что проведение такого лечения возможно только в хорошо оснащённых, укомплектованных квалифицированными специалистами ожоговых центрах.
СПИСОК ЛИТЕРАТУРЫ
- Алексеев А.А., Кудзоев О.А., Сарыгин П.В./ Рациональная пластическая хирургия локальных глубоких ожогов и отморожений // Мат. науч. конф.: «Актуальные проблемы травматологии и ортопедии». – Н.Новгород, 2001 – C. 69-70
- Алексеев А.А., Ю.И. Тюрников/ Статистические показатели ожоговых стационаров Российской Федерации за 2013 год // Мат. науч. конф.: «Ожоги и медицина катастроф». – Уфа, 2014 – C. 16-18
- Арьев Т.Я/ Термические поражения. //– Л. : Медицина, 1966. – 704 с
- Вихриев Б.С., Бурмистров В.М./ Термические поражения.//– Л.: Медицина, 1985. – 208 с
- Гусак В.К., Фисталь Э.Я., Баринов Э.Ф., Штутин А.А. /Термические субфасциальные поражения.//Донецк, 2000 – 181 c
- Евтеев А.А., Тюрников Ю.И./ Неудачи аутодермопластики // М.: РА ИЛЬФ, 2011. – 160 с
- Кичемасов С.Х./ Кожная пластика лоскутами с осевым кровоснабжением при термических поражениях IV степени: автореф. дис. д-ра мед. наук //— Л., 1990 —48 с
- Колесников И. С., Вихриев Б. С./ Оперативное лечение глубоких термических ожогов //– М.: Медгиз, 1962 – 179 с
- Малютина Н.Б./ Сравнительная оценка эффективности различных методов оперативного лечения обожженных пожилого и старческого возраста : дис. канд. мед. наук. М., 2002. – 134 с
- Матвеенко А.В., Чмырѐв И.В., Петрачков С.А./ Определение тяжести состояния обожженных с помощью координатных сеток вероятности летального исхода // Скорая помощь: Рос.науч.-практ. журн. – СПб., 2013. – Т.14, № 1. – С. 34-43
- Ожоги: руководство для врачей./ Я.О. Порембский, Б.А. Парамонов, В.Г. Яблонский. – СПб.: СпецЛит, 2000 – 488с
- Соколов В.А. Комбинированная ауто-аллодермопластика в лечении обожженных : автореф. дис. … канд. мед. наук. – СПб.,1995. – 22 с
- Тюрников Ю.И., Сухов Т.Х., Евтеев А.А./ Опыт хирургического лечения больных с критическими ожогами./ Мат. науч. конф.: «Ожоги и медицина катастроф». – Уфа, 2014 – С.204-206
- Чмырев И.В./ Некрэктомия у обожженных: Инновационные подходы при оказании специализированной медицинской помощи.: дис. д-ра мед. наук. СПб., 2014. – 301 с
- Шаповалов С.Г. Оперативное лечение пострадавших от ожоговой травмы в чрезвычайных ситуациях / С.Г. Шаповалов, А.Н. Белых // Вестн. Национального медико-хирургического центра им. Н.И. Пирогова. — 2011. – Т. 6, № 1. –С. 67-76.
- Шаповалов С.Г., Плешков А.С., Панов А.В., Мельникова О.А., Сухопарова Е.П., Новицкая А.А./ Организация оказания медицинской помощи пациентам на базе ожогового отделения. Первый опыт применения МЕЕК методики в России./ Мат. науч. конф.: «Ожоги и медицина катастроф». – Уфа, 2014 – С.79-81
- Bishara SA, Shady NH, Gunn SW /New technologies for burn wound closure and healing. Review of the literature. Burns 31 (2005): p944–956
- Burke JF, Bondoc CC, Quinby WC /Primary burn excision and immediate grafting: a method shortening illness // J. Trauma– Vol. 14, № 5(1974): p389 – 395
- Caldwell FT Jr, Wallace BH, Cone JB /Sequential excision and grafting of the burn injuries of 1507 patients treated between 1967 and 1986: end results and the determinants of death.// J Burn Care Rehabil 17(1996): p137–146
- Cole JK, Engrav LH, Heimbach DM, Gibran NS, Costa BA, Nakamura DY, Moore ML, Blayney CB, Hoover CL/ Early excision and grafting of face and neck burns in patients over 20 years./ Plast Reconstr Surg 109(2002): p1266–1273
- Davis SC, Mertz PM, Bilevich ED et al /Early debridement of second degree burn wounds enhances the rate of reepithelialization – an animal model to evaluate burn wound therapies.// J Burn Care Rehabil 17(1996): p558–561
- Deitch EA, Wheelahan TM, Rose MP, Clothier J, Cotter J/ Hypertrophic burn scars: analysis of variables.// J Trauma 23(1983): p895–898
- Domres B, Kistler D, Rutczynska J/ Intermingled skin grafting: a valid transplantation method at low cost.// Annals of Burns and Fire Disasters — vol. XX — n. 3 — September 2007: p 149-154
- Gore DC, Chinkes D, Heggers J, Herndon DN, Wolf SE, Desai M./ Association of hyperglycemia with increased mortality after burn injury.// J Trauma 2001; 51: p540-544
- Jackson DM/ The diagnosis of the depth of burning// Br J Surg 40(1953): p588–596
- Jackson DM/ Second thoughts on the burn wound// J Trauma 9(1969): p839–862
- Janzekovic Z/ A new concept in the early excision and immediate grafting of burns// J Trauma 10(1970): p1103–1108
- Jeffrey SLA/ Debridement of pediatric burns. In: Granick MS, Gamelli RL (eds) Surgical wound healing and management.// Informa Health Care (2007), USA: p53–56
- Heimbach DM/ Early burn excision and grafting // Surg. Clin. North Am– Vol. 67, № 1(1987): p93-107
- Herndon DN, Barrow RE, Rutan RL, Rutan TC, Desai MH, Abston S /A comparison of conservative versus early excision. Therapies in severely patients // Ann. Surg. – Vol. 209, №5(1989): p547-552
- Herndon DN, Parks DH/ Comparison of serial debridement and autografting and early massive excision with cadaver skin overlay in the treatment of large burns in children.// J. Trauma.– Vol. 26, № 2(1986): p149-152
- Kara M, Peters WJ, Douglas LG, Morris SF / An early surgical approach to burns in the elderly// J. Trauma — Vol. 30, №4 (1990): p430-432
- Kreis RW, Mackie DP, Vloemans AW/ Widely expanded postage stamp skin grafts using a modified Meek technique in combination with an allograft overlay.// Burns, 19(1993): p142-145
- Lanz O/ Dei Transplantation Betreffend.// Zentralbl f Chir 35(1908): p 3
- Lin TW, Horng SY /The algebraic view-point in microskin grafting in burned patients// Burns.–Vol. 20, №4 (1994): p347-350
- Lumenta DB, Kamolz LP, Keck M et al./ Skin expansion rates and its results by the use of mesh and micrografting techniques.// 43rd Annual Meeting of the American Burn Association, Chicago, J Burn Care Res, 32(2011) S155
- Magliacani G/ The surgical treatment of burns: skin substitutes./ Annals of the MBC — vol. 3 — September 1990: p145-160
- Mathes S, Nahai F./ Clinical application for muscle and musculocutaneous flaps.// Mosby, St Louis, 1982: 3
- Maungman P, Sullivan SR, Honari S, Engrav LH, Heimbach DM, Gibran NS /The optimal time for excision in major burn injury //J. Med. Assoc. Thai. – 2006. – Vol. 89, № 1: p29-36
- Meek CP/ Successful microdermagrafting using the Meek-Wall microdermatome.//Am. Surg. vol. 29(1958): p.61
- National Burn Repository 2013. American Burn Association. Version 9.0. All Rights Reserved Worldwide. 311 S. Wacker Drive Suite 4150 Chicago, IL 60606 312-642-9260 www.ameriburn.org
- Palmieri TL, Greenhalgh DG/ Topical treatment of pediatric patients with burns: a practical Guide.// Am J Clin Dermatol 3(2002): p529–534
- Paul J. Kim, DPM, Karolina S. Dybowski, BS, and John S. Steinberg/ A Closer Look At Bioengineered Alternative Tissues.// Podiatry today. Volume 19 — Issue 7 — July 2006, p38-55
- Rennekampf HO, Tenenhaus M/ Debridement of the burn wound.// In: H. Hyakusoku et al. (eds.) Color Atlas of Burn Reconstructive Surgery/ Springer-Verlag Berlin Heidelberg 2010: p10-15
- Rosenberg L et al. Safety and efficacy of a proteolytic enzyme for enymatic burn debridement: a preliminary report. Burns 2004;30: p843–850
- Singer AJ., Taira BR, Anderson RB, McClain SA, Rosenberg L./Reepithelialization of Mid-dermal Porcine Burns After Rapid Enzymatic Debridement With Debrase.// J Burn Care & Research: November/December 2011 — Volume 32 — Issue 6: p 647-653
- Böttcher-Haberzeth S, Biedermann T, Reichmann E / Tissue engineering of skin//Burns 36 (2010): p450-460
- Steadman PB, Pegg SP /A quantitative assessment of blood loss in burn wound excision and grafting.// Burns 18 (1992): p490–491
- Surgical Management of the Burn Wound and Use of Skin Substitutes/ Kagan RJ et al (eds.)/ //American Burn Association White Paper, 2009: 50p
- Tompkins RG, Remensnyder JP, Burke JF, et al./Significant reductions in mortality for children with burn injuries through the use of prompt eschar excision//Ann Surg. 208(5) Nov 1988: p577-585
- Wood FM, Kolybaba ML, Allen P/ The use of cultured epithelial autograft in the treatment of major burn injuries: A critical review of the literature// Burns, June 2006 — Volume 32, Issue 4: p395-401
- Zhang ML, Wang CY, Chang ZD et al. /Microskin grafting. Clinical report.//Burns, 12(1986): p544-548