
ОБЪЕДИНЕНИЕ КОМБУСТИОЛОГОВ
«МИР БЕЗ ОЖОГОВ»
Профилактика гнойно-некротических осложнений у пострадавших от высоковольтных электроожогов верхних конечностей
Солошенко В.В.
Фисталь Н.Н.
Отдел термических поражений и пластической хирургии института неотложной и восстановительной хирургии АМН Украины. г.Донецк.
Высоковольтный электроожог является одной из тяжелейших травм. При прохождении электрического тока через ткани верхней конечности происходит повреждение глубоких анатомических структур, в частности больших мышечных массивов. Наличие погибших мышц под неповрежденной кожей является одной из причин развития гнойно-некротических осложнений [1]. Поэтому, определение жизнеспособности скелетных мышц в зоне поражения в ранние сроки после травмы является проблемой для комбустиологов, сосудистых хирургов и травматологов [2]. Регистрация биоэлектрической активности мышцы позволяет определить ее жизнеспособность. Электромиография применяется для оценки состояния мышцы и нервов во многих областях медицины [3,4,5], однако, мы не обнаружили сведений о применении метода ранней диагностики жизнеспособности мышечной ткани у обожженных, путём проведения игольчатой электромиографии.
Для определения жизнеспособности мышечной ткани и степени поражения нервно-мышечного комплекса применялась игольчатая миография. С этой целью использовали игольчатые электроды электромиографа «Reporter» итальянской фирмы «EsaoteBiomedica». Для точности определения глубины поражения на электрод были нанесены миллиметровые деления. Жизнеспособность мышцы изучалось в трех состояниях — биоэлектрическая активность при введении иглы (всплеск биоэлектрической активности в момент введения электрода), в состоянии покоя (в норме в здоровой расслабленной мышце биоэлектрическая активность не регистрируется), а так же — при произвольном напряжении мышцы Электрические потенциалы мышечных волокон регистрировались и обрабатывались на четырёхканальном электромиографе, что позволило визуализировать потенциал двигательной единицы, сравнивать и накапливать материал. Изучение параметров потенциалов при отведении их игольчатыми электродами производилось нами при скорости развёртки 10 мс и усилении 200 мкВ на деление экрана, что облегчает визуальное сравнение результатов исследования. Диапазон частот усилителя, необходимый для неискаженной регистрации потенциалов при игольчатом отведении, находится в пределах от 2 до 20000 Гц. При одном введении электрода исследовали ряд участков мышцы, перемещая электрод в различных направлениях и на нескольких уровнях. Согласно методике, описанной в руководстве по электромиографии и электродиагностике Х.Коуэна и Дж. Брумлика (1975 г.), удобным является способ «четырёх квадрантов» [3], заключающейся в проведении исследования в четырёх направлениях и на трёх уровнях. Биполярный концентрический игольчатый электрод вводился в пораженный сегмент, при этом погибшие мышцы не имели биоэлектрической активности. На мониторе не определялось какого-либо вида биоэлектрической активности — отмечалось «биоэлектрическое молчание» (рис.1). Как только электрод входит в жизнеспособную мышечную ткань — появлялись потенциалы двигательной единицы мышечных волокон или потенциалы различного вида спонтанной активности — потенциалы фасцикуляции, фибриляции (рис.2). Электроды вводили через каждые 10 мм, по всему объёму мышцы или мышечного массива, согласно топическому расположению мышцы. Диаметр регистрирующего электрода — 0,45-0,65 мм, длина 32 мм, что позволяло точно определять границы жизнеспособной мышцы.

Рис.1. Биоэлектрическое молчание.
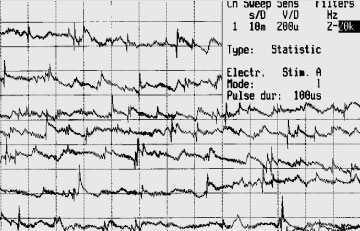
Рис.2. Биоэлектрическая активность жизнеспособной мышцы.
Важнейшим условием для получения верных результатов была предварительная оценка состояния иннервации при помощи стандартных методик. В случае нарушении целостности двигательного нерва в начальных стадиях в мышце наблюдался период биоэлектрического «молчания», что может быть неверно истолковано и повлечь за собой ошибку. В данной ситуации мы использовали, дополнительную методику, которая заключалась в подаче на мышцу стимулирующего импульса. Наиболее простым стимулирующим игольчатым электродом является обычная инъекционная игла, используемая нами в качестве катода, которая легко проникает сквозь некротический струп. Анодом в этом случае служит пластинчатый электрод. Амплитуда выходного импульса стимулятора регулировалось по напряжению, длительность выходного импульса от 1000 микросекунд, частота импульсов -1 импульс в секунду, что было обусловлено значительной рефрактерностью мышц в зоне поражения. Регистрирующий электрод последовательно вводили в мышцу по описанной ранее методике, начиная с заведомо пораженного участка мышцы и выявляли границу поражения по появлению биоэлектрической активности. Кроме того, игольчатая миография использовалась для изучения динамики восстановления функции мышцы после перенесенной травмы, для контроля процесса реиннервации мышц после реконструктивных операций. (Патент Украины N 25468 А, МПК А 61 В 6/00).
На основании данных электрофизиологического исследования производили некрэктомию следующим образом: Мышцы, не имеющие биоэлектрической активности, удалялись полностью. Если мышца поражалась не на всю толщину, — тангенциально иссекался участок соответствующий зоне биоэлектрического молчания (рис.3.).
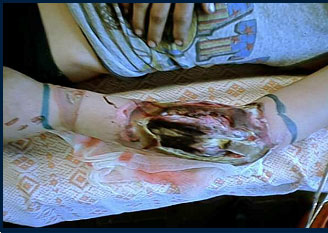
Рис.3. Зона гибели мышц верхней конечности в результате высоковольтного электроожога, выявленная методом игольчатой электромиографии.
При проведении тангенциальной некрэктомии мы старались сохранить перимизий как источник регенерации. Если полностью погиб участок мышцы на протяжении, мышцу иссекали на зажимах, оставляя в ране её дистальный и проксимальный концы. После иссечения участка погибшей мышцы, культя её прошивались кетгутом. Если рядом находились неповрежденные мышцы синергисты, — оставшийся после некрэктомии дистальный или проксимальный конец иссеченной мышцы фиксировали к мышце синергисту или её сухожилию (рис.4,5.).
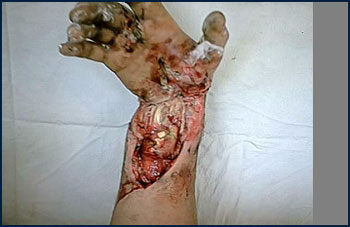
Рис.4. Высоковольтный электроожог ннижней трети правого предплечья после удаления кожного струпа.
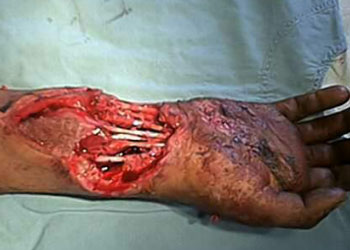
Рис.5. Рана нижней трети правого предплечья после проведения некрэктомии
Для изучения эффективности диагностики повреждения, в частности, разработанного нами электрофизиологического способа определения жизнеспособности мышечной ткани были выделены две группы больных. В первую группу (основная группа наблюдения) вошли пострадавшие с обширным поражением нервно-мышечного комплекса верхней конечности, находившиеся на лечении в ожоговом центре с 1998 по 2000 год (29 человек), которым использовали данный метод диагностики. Вторую группу (группу контроля) составили больные с аналогичными поражениями как по площади, так и по локализации, находившиеся на лечении в клинике до 1998 года (29 человек), когда описанный метод диагностики жизнеспособности мышечной ткани ещё не применялся. Больным в обеих групп выполнялись как операции с применением васкуляризированных лоскутов, так и свободных расщепленных аутолоскутов. Группы сопоставимы по параметрическим и непараметрическим признакам.
Проведен сравнительный анализ результатов лечения в группе контроля и группе наблюдения, в которой использован разработанный и предложенный нами способ диагностики жизнеспособности мышечной ткани. Выявлено, что длительность пребывания в ожоговом центре в группе больных, где применялась электромиографическая диагностика жизнеспособности мышц руки, составила в среднем 36,79 + 2,01 суток, а в группе контроля, где жизнеспособность мышц оценивалась визуально во время операции, длительность пребывания больного в стационаре составила 46,59 + 3,02 суток. (F=2,25 p=0,035), то есть в группе наблюдения длительность лечения в ожоговом центре была меньше на 9,8 дня чем в группе контроля. Уменьшение длительности пребывания больного в стационаре достигнуто, по нашим данным, за счет своевременной и точной диагностики повреждения мышц, оптимизации течения раневого процесса, в частности — уменьшения числа гнойных осложнений.
В обеих группах выполнялись аналогичные оперативные вмешательства, однако, благодаря своевременной диагностике зоны гибели мышечной ткани, удалось уменьшить число проводимых повторных некрэктомий. В группе наблюдения количество некрэктомий на одного больного составило 2,8 + 0,27, в то время как в группе контроля — 3,79 + 0,76 (F=4,23 р=0,01), то есть в группе контроля число некрэктомий на одного больного достоверно больше. Количество таких оперативных вмешательств, как вскрытие гнойных затеков оказалось значительно меньше в группе наблюдения (соответственно 2 и 9 операций) чем в группе контроля, где не проводилась оценка жизнеспособности мышечной ткани по предложенному способу (c 2 = 8,32 p = 0,02, то есть в группе контроля гнойно-некротических осложнений было достоверно меньше). Снижение числа гнойных осложнений позволило проводить в более ранние сроки пластику дефектов верхней конечности путем свободной аутодермопластики. Так, в группе наблюдения первая свободная аутодермопластика выполнялась на 8,1 + 1,21 сутки, а в группе контроля на 15,86 + 1,89 сутки (F = 2,43 р = 0,021), то есть в группе наблюдения первая аутодермопластика выполнялась значительно раньше, в среднем на 7,7 суток. Следовательно, радикально проведенная некрэктомия позволяет подготовить в более короткие сроки рану для последующей пластики.
Во время выполнения ампутации сегментов руки (плечо и предплечье) в группе контроля не всегда удавалось четко визуально определить границу погибших мышц, поэтому возникала необходимость в проведении реампутации. Применение электрофизиологического метода определения жизнеспособности мышечной ткани позволило резко сократить количество подобных оперативных вмешательств.
Количество реампутаций предплечья в группе наблюдения по сравнению с группой контроля снизилось в 6 раз, количество реампутаций плеча в 4 раза. Данный факт свидетельствует об эффективности предложенного метода диагностики жизнеспособности мышечной ткани.
Таким образом, профилактикой гнойно-некротических осложнений при высоковольтных электрических ожогах, сопровождающихся гибелью мышц руки, является ранняя некрэктомия, основанная на данных электромиографического исследования.
Список литературы
- Фисталь Э.Я. Диагностика и хиругическое лечение электрических ожогов: Дис… канд. мед. наук: 14.00.27. — Донецк, 1988. — 179 с.
- Термические субфасциальные поражения / Гусак В.К., Фисталь Э.Я., Баринов Э.Ф., Штутин А.А. — Донецк: Донеччина, 2000. — 192 с.
- Коуэн, Брумлик К. Руководство по электромиографии и электродиагностике. — М.: Медицина, 1975. — 192с.
- Электромиография в диагностике нервно-мышечных заболеваний / Гехт Б.М., Касаткина Л.Ф., Самойлов М.И., Санадзе М.И., Санадзе А.Г. / Таганрог: Изд-во ТРТУ, 1997. — 370 с.
- Wiedemann E., Eggert C., Illert M., Stock W., Wilhelm K. Functional electromyography analysis of radial replacement operation // Orthopade. — 1997. — Vol.26, N8, P.673-683.
Designed by Сайт на Заказ