ОБЪЕДИНЕНИЕ КОМБУСТИОЛОГОВ
«МИР БЕЗ ОЖОГОВ»
Микрохирургическая аутотрансплантация тканей при обширных рубцовых деформациях и контрактурах шеи
Юденич А.А.
Сарыгин П.В.
Кафаров Т.Г.
Попов С.В.
Институт хирургии им.А.В.Вишневского РАМН, Москва.
Вступление
Коррекция обширных рубцовых деформаций шеи является одной из сложных проблем реабилитации больных с последствиями ожоговой травмы. Для их ликвидации используются все известные способы восстановительно-пластических операций. Однако, несовершенство предложенных методов заставляет хирургов разрабатывать новые более эффективные способы хирургического лечения.
С внедрением в клиническую практику микрохирургической аутотрансплантации тканей появились новые возможности улучшения результатов операций этой тяжелой группы больных (А.А.Юденич, Ж.О.Белеков, 1990; Ж.О.Белеков 1990; G.F.Nappi, Lubbrts S.M., 1986; K.Kobus, I.Stepniewski 1988; D.Boucq et al., 1988).
Для устранения послеожоговых рубцовых деформаций и контрактур шеи хирургами применяются различные способы пластических операций, в частности, свободные кожно-фасциальные лоскуты. Однако, размеров этих лоскутов нередко оказывается недостаточно для закрытия обширной раны на шее и проведения адекватной коррекции контрактуры. С целью увеличения размеров переносимых лоскутов применяется метод дозированного растяжения тканей экспандерами (М.М.Мадазимов, В.Ю.Мороз, А.А.Юденич, 1989; В.Ю.Мороз, А.А.Юденич, Т.Г.Кафаров и соавт., 1990).
Материалы и методы
В течениии 10 лет в отделении реконструктивной и пластической хирургии оперировано 268 больных с послеожоговыми рубцовыми деформациями и контрактурами шеи. Мужчин было 133, женщин — 135. Возраст большинства пациентов (75,2%) составлял от 20 до 55 лет. Основной этиологической причиной, приведшей к рубцовым деформациям и контрактурам была термическая травма. Сроки выполнения пластических операций колебались от 8 до 13 лет после заживления ожоговых ран.
Для коррекции рубцовых стяжений шеи у 205 больных мы использовали неповрежденную кожу надплечий, боковых поверхностей шеи, переднего и боковых отделов грудной стенки в виде кожно-жировых и кожно-фасциальных лоскутов… эполетных, шейных, шейно-грудных, плечегрудных, подмышечно-грудных.
У 63 пациентов послеожоговые деформации шеи сочетались с повреждением надплечий и грудной стенки. Последнее обстоятельство не позволяло использовать для пластики кожу этих областей. Для реабилитации этой группы больных применялся метод микрохирургической аутотрансплантации нерастянутыми тканями (таблица N 1).
|
Таблица N 1 |
||
| Вид лоскута | Нерастянутый | Растянутый |
| Лопаточный | 15 | 30 |
| Дельтовидный | 5 | - |
| Лучевой | 3 | - |
| Всего: | 23 | 30 |
Как видно из таблицы, методы тканевого дозированного растяжения тканей использовался только при пластики лопаточныи лоскутом.
Пластические операции при ликвидации послеожоговых рубцовых деформаций шеи нерастянутыми микрохирургическими лоскутами не отличались от классической схемы. В качестве реципиентных сосудов у 31 больного использовалась лицевая артерия и вена, а у двух пациентов — общая сонная артерия и наружная яремная вена. Одним из определяющих факторов в профилактике тромбообразования является рациональное расположение микрососудистых анастомозов. Сдавление окружающими тканями, небольшой переркут, перегиб анастомозов приводит к недостаточности кровообращения в лоскуте и увеличивает риск образования тромба, особенно в венозных анастомозах.
После анастомозирования сосудов производили моделирование лоскута к краям раны на шее. Для лучшей адаптации пересаженных тканей и герметизации подлоскутного пространства накладывали два ряда швов с обязательным дренированием вакуумной системой.
Метод тканевого растяжения и пластика обширных деформаций шеи растянутым лопаточным лоскутом
Для увеличения размеров сложно-составного лоскута использовали отечественные латексные экспандеры. Прирост площади растягиваемых тканей достигал 100-150 %.
Требования, предъявляемые к использованию зонам расширения были следующими:
- Кожа растягиваемого участка должна быть неповрежденной.
- Кожа растягиваемого участка по качественным характеристикам (цвету, текстуре, типу оволосенения) должна соответствовать коже предполагаемой трансплантации.
- Для закрытия обширной раны на шее нужен точный расчет площади переносимых тканей, которые должны соответствовать или превышать размеры дефекта на шее.
По нашему мнению лучшей зоной, отвечающей указанным требованиям является лопаточная. Лопаточный лоскут имеет анатомические параметры схожие с кожей шеи. Кроме того, его особенность состоит в том, что питающие сосуды проходят в поверхностной фасции спины. Это обстоятельство позволяет имплантировать экспандер в бессосудистом межфасциальном пространстве и безопасно выполнять мобилизацию экспандера.
Техника имплантации экспандеров
Область лопатки условно разделяли на четыре квадранта. Намечали линию разреза, который проходил паралельно задней подмышечной линии, отступя от края лопатки на 22-23 см. Производили разрез кожи, подкожной клетчатки, фасции. Тупым и острым путем выделяли бессосудистую зону размером 6-14 см. Границами её являются… медиально — позвоночник, сверху — ость лопатки, снизу — нижний её угол. В сформированный карман имплантировали экспандер, заполненный 20-30 мл раствора фурацилина. Клапанную трубку оставляли под кожей. Дозированное растяжение тканей производили в течении 3-4 недель. Количество вводимой жидкости зависело от объема экспандера (до 1500 мл).
После достижения нужных размеров растянутого лоскута, иссекали рубцы на шее, устраняли контрактуру. Удаляли экспандер.
Мобилизацию лоскута начинали от периферии к центру, т.е. до выхода артерии, окружающую лопатку из трехгранного отверстия. При этом оставляли участок растянутых тканей, примерно 1-2 см, со стороны параскапулярной области для закрытия обширной донорской раны. Значительные трудности возникали при выделении сосудистого пучка. В месте выхода нисходящей ветви артерии, окружающей лопатку соединительнотканная капсула, образовавшаяся вокруг экспандера, всегда утолщена, интимно спаяна с тканями, обильно кровоточит, что не сразу позволяло определить расположение сосудов. С целью предупреждения их повреждения в области сосудистой развилки в лоскут включали часть капсулы в виде муфты. После мобилизации лоскута его оставляли на сосудистой ножке и определяли транскутанное насыщение кислорода. Обширную донорскую рану ушивали, используя в качестве дополнительного пластического материала оставшиеся растянутые ткани. Лоскут переносили на рану шеи. Микроанастомозы накладывали по общепринятой методики наложения микрососудистого шва. Растянутыми тканями лопаточного лоскута удавалось закрывать раны шеи от подбородочной области до ключиц.
Электронно-радиографическое исследование растянутой кожи не показало существенных отличий от нормальной. Не выявлено морфологических изменений, которые могли бы привести к ухудшению трофических свойств кожи. Дерма растянутой кожи богата сосудами, большая часть которых находится в функционально активном состоянии. Увеличение количества сосудов в растянутой дерме имеет решающее значение, так как, они являются важнейшей структурной и функциональной единицей тканей, обеспечивающей не только кровоснабжение, но и их рост. Следовательно, растянутая кожа, может быть, использована в качестве пластического материала.
Результаты
Осложнения, возникшие в процессе тканевого растяжения наблюдались нами у 3 пациентов. У одного больного отмечено нагноение гематомы в ложе экспандера. Ложе было дренировано, промывалось растворами антисептиков. Больной получал антибактериальную терапию в соответствии с чувствительностью микрофлоры. Предпринятые лечебные мероприятия позволили купировать воспалительные явления и закончить процесс тканевого растяжения. Пролежень над куполом тканевого расширителя отмечен у одного пациента. Это потребовало остановить растяжение на 10 дней. После чего тканевое растяжение было продолжено. У третьего больного произошел спонтанный разрыв экспандера из-за дефекта в нем. Выполнена реимплантация нового тканевого расширителя и растяжение было продолжено.
Осложнения в виде тромбоза артериальных и венозных анастомозов отмечено у 10 из 63 оперированных больных. Все пациенты экстренно оперированы. Успешное реанастомозирование выполнено у 3 больных.
В отдельные сроки после операции (4 года) выявлено, что кожа нерастянутых и растянутых лоскутов сохраняет все свои свойства. Лоскуты были подвижны, мягкими, легко брались в складку. Отмечалось увеличение лоскутов на 30-40 % от первоначального размера. Однако у 12 (19 %) больных отмечена сглаженность шейно-подбородочного угла за счет избытка подкожно-жировой клетчатки и развитие гипертрофических и келоидных рубцов по краям пересаженного лоскута, что потребовало повторных коррегирующих операции. Рецидивов контрактур не выявлено.
Обсуждение
Показанием к использованию сложно-составных лоскутов на микрососудистых анастомозах является наличие обширных рубцовых деформаций и контрактур шеи при отсуствии неповрежденной кожи шеи, надплечий и грудной стенки. Проведение аутодермопластики при рубцовом поражении шеи часто бывает неэффективно и приводит к рецидиву ограничений движений. В таких условиях применение микрохирургических кожно-фасциальных лоскутов позволяет успешно решить задачу полного восстановления движений шеи и воссоздания кожного покрова, близкого к естественному.
Метод предварительного дозированного растяжения свободных кожно-фасциальных лоскутов существенно улучшает результаты реконструктивных операций за счет возможности более широкого удаления рубцовопораженных тканей. Наиболее удобен для этой цели, по нашему мнению, лопаточный лоскут по своим свойствам близкий к коже шеи.
Безусловно, эстетический результат операций зависит от индивидуальных особенностей пациентов. Так, у ряда тучных больных, избыточное количество подкожно-жировой клетчатки в лоскутах потребовало их последующего обезжиревания. Которое мы проводим в сроки от 3 месяцев после трансплантации микрохирургического лоскута. Сложной проблемой стало образование гипертрофических и келоидных рубцов по краям пересаженного лоскута, которые наблюдались нами у 25 % больных. У пациентов, склонных к келоидозу, практически было невозможно предотвратить образование патологических рубцов. Поэтому в таких случаях мы назначали после оперативных вмешательств физиотерапевтическое и бальнеологическое лечение, внутрирубцовое введение кеналога.
Несмотря на то, что латексный экспандер оказывает механическое воздействие на все структуры кожи, ее параметры оставались в пределах нормы. Это показало проведенное электронно-радиографическое исследование растянутых тканей. Визуально растянутая кожа лопаточного лоскута, также не отличалась от обычной. Она сохраняла свой цвет, эластичность, текстуру.
Степень успеха проведенных реконструктивных операций по поводу обширных рубцовых деформаций и контрактур шеи определяется несколькими показателями — первичным приживлением тканей лоскута, его хорошим внешним видом, восстановлением движений головы в шейном отделе позвоночника, возможностью пациента вернуться к прежнему образу жизни.
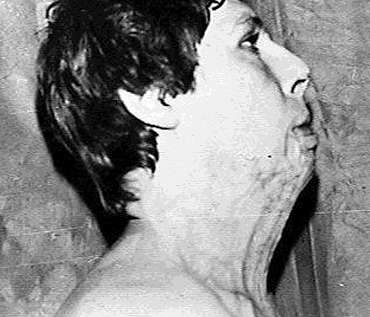
Рис.1 Вид послеожоговой рубцовой контрактуры шеи до операции.
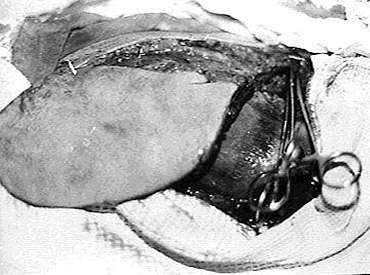
Рис.2 Вид растянутого экспандерами лопаточного лоскута после его мобилизации.
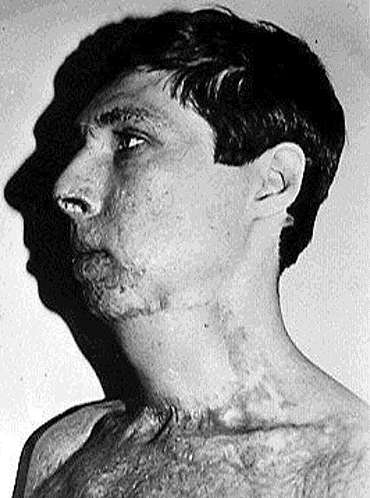
Рис.3 Вид шеи после пластики растянутым лопаточным лоскутом на микрососудистых анастомозах.
Список литературы
- Белеков Ж.О. Коррекция послеожоговых рубцовых дефектов и рубцовых деформаций шеи и конечностей свободным лоскутом на микрососудистых анастомозах — Автореф.дис…канд.мед.наук…. М., -1990 — 19 с.
- Мадазимов М.М., Мороз В.Ю. , Юденич А.А. Пластика послеожоговых рубцовых деформаций и контрактур шеи расширенным лопаточным лоскутом на микроанастомозах — Актуальные вопросы реконструктивной и восстановительной хирургии — Тез.докл. — Иркутск — 1989 — с.228.
- Мороз В.Ю., Юденич А.А., Кафаров Т.Г., и др. Пластика послеожоговых рубцовых деформаций шеи растянутым лопаточным лоскутом на микрососудистых анастомозах — Хирургия — 1990 — N 9 — с.135-139.
- Юденич А.А., Белеков Ж.О. Пластика шеи лопатчным лоскутом га микрососудистых анастомозах — Вестн.хирургии — 1990 — N 12 — с.74-77.
- Boucq D., Schoofs M., Fissette I. Reconstruction cervicale, apres brulleres, par lambeau libre parascapulare — Ann.Chir.Plast.Esthet. -1988 — N 33 -p.315-320.
- Kobus K., Stepnewski S. Surgery of postburn contractures — Eur.J.Plast.Surg. — 1988 — Vol. 11 — N 2 — p.126-131.
- Nappi G.F., Lubberts S.V. Composite tissue transfer in burn patients. — Clin.Plast.Surg. — 1986 — Vol.13 — N 1 — p.137-142.
Designed by Сайт на Заказ