ОБЪЕДИНЕНИЕ КОМБУСТИОЛОГОВ
«МИР БЕЗ ОЖОГОВ»
Роль изучения процесса адаптации на ожоговую рану
Ушакова Т.А.
Научно-практический центр термических поражений МЗ и СР РФ Института хирургии им. А.В. Вишневского РАМН, г.Москва.
Термическая травма — один из сильнейших стрессов, испытуемых человеком. В ответ на повреждение в организме развивается системная ответная реакция (общий адаптационный синдром), включающая несколько стадий: шока, срочной адаптации и истощения. Термин срочная адаптации подразумевает спад стрессовой реакции и восстановление утраченных функций систем и органов до исходного уровня. Изучение адаптивных реакций организма является крайне важным, т.к. предполагает определение соответствия уровня мобилизации организма степени тяжести травмы, времени наступления срочной адаптации или ее срыва, влекущего за собой развитие метаболического истощения, полиорганной недостаточности и сепсиса.
Актуальность проведенного исследования диктовалась, прежде всего, наличием односторонней тенденции в оценке состояния больного: с позиций развития патологии. Однако, Д.С. Саркисов (1987), а еще ранее И.В. Давыдовский (1969), отводили центральное место в физиологии и патологии проблеме компенсации нарушенных функций. В своих исследованиях мы все глубже проникаем в молекулярные механизмы патогенеза. Описаны десятки и сотни медиаторов, цитокинов, промежуточных продуктов метаболизма. Но, к сожалению, мы практически не обращаем внимания на закономерности ответной реакции организма на повреждение, т.е., на процесс восстановления.
Своего рода методологическим инструментом для решения этой проблемы может быть принципиально иной подход в оценке состояния больного — с позиций теории H. Selye о стрессе и общем адаптационном синдроме. Рассматривая ожоговую болезнь как каскад острых и хронических стрессовых факторов, мы можем и должны исследовать две стороны процесса: степень повреждения и степень мобилизации организма для ответа на это повреждение. Соответственно, в дальнейшем мы сможем более тонко манипулировать лечебными мероприятиями, воздействуя на оба противоборствующих начала: не только стараться нейтрализовать патологию, но и ускорять процесс адаптации, повышать метаболические ресурсы организма.
В результате обследования тяжелообожженных пациентов изучен характер протекания стрессовой реакции и выявлены ее особенности, определены биохимические критерии срочной адаптации и прогностически неблагоприятные признаки.
Под наблюдением находились пострадавшие (70 человек) с площадью глубоких ожогов 15 и более % поверхности тела в острый период ожоговой болезни. Программа анализа включала: определение фона кортикостероидов; состояние про- и антиоксидантной систем: по продуктам тиобарбитуровой кислоты (ТБК), показателю хемилюминесценции (ХЛ), активности каталазы, железосвязывающей способности организма (ЖСС), сывороточному содержанию железа, меди; исследование белкового обмена с определением азотистого баланса; углеводного и жирового: по содержанию глюкозы, общего холестерина, триглицеридов, лиопротеидов высокой плотности (HDL); а также мы исследовали уровень молекул средней массы (МСМ); оценивали иммунограмму с определением клеточных и гуморальных факторов, индекса фагоцитоза, циркулирующих иммунных комплексов (ЦИК), лизоцима.
Кратность исследований — 4-5 раз, периодичность — 5-7 дней. Сроки — период стрессовой реакции: с момента получения травмы до относительного восстановления исходного гомеостаза, т.е. период достижения срочной адаптации.
В результате изучения этого периода у пациентов с тяжелой термической травмой выявлены следующие особенности протекания стрессовой реакциии:
- волнообразный характер динамики метаболических показателей по типу маятника, размах которого, отражающий степень дисбаланса, коррелирует с тяжестью состояния пациента.
- наличие корреляционных связей показателей, как прямых, так и обратных. Например, повышение уровня экскреции стрессовых гормонов влечет за собой увеличение катаболизма аминокислот, показателя ХЛ, ТБК-продуктов, снижения HDL, повышение активности каталазы. Чем больше содержание сывороточной меди, тем выше индекс фагоцитоза и т.д. При утяжелении состояния больного эти связи ослабевают и, наконец, исчезают совсем.
- повышенный фон кортикостероидов у всех тяжелообожженных больных на протяжении 4-5 недель после травмы, что свидетельствует о продолжающемся формировании ответной реакции на стресс. Однако у наиболее тяжелых пациентов происходит быстрый спад гормонального фона в более ранние сроки (до относительной компенсации состояния), что требует соответствующей и своевременной коррекции. Выявлено преимущественное усиление экскреции метаболитов оксикортикостероидов, нарушается соотношение фракций 17ОКС/17КС как ¼.
- длительно существующий отрицательный азотистый баланс. Причем, по азоту мочевины нормализация происходит в течение нескольких суток, в то время как повышение экскреции азота аминокислот — патогномоничный симптом гиперкатаболизма, продолжается вплоть до выписки больного. Получены также практические данные по коррекции гипопротеинемии растворами аминокислот. Для тяжелообожженных пациентов характерны умеренные гипераминоацидемиия (до 11 мг%) и гипераминоацидурия (до 1000мг/сут), причинами которых являются: неспособность печени и почек в условиях энергетического дефицита метаболизировать экзогенные АК, нарушение реабсорбции АК почками в связи с наличием нефропатии и избыточное введение АК, которые резко усиливают азотемию и его экскрецию.
- гипохолестеринемия и триглицеридемия на фоне значительного снижения уровня HDL (липопротеидов высокой плотности), который является косвенным антиоксидантом и показателем синтетической функции печени. Оказалось, что этот параметр коррелирует со степенью тяжести пациента.
- истощение в про- и антиоксидантной системе. Изначально выявлено умеренное преобладание первой в течение короткого острого периода, причем, далеко не у всех больных. У тяжелообожженных наблюдается быстрое истощение обеих систем: незначительное повышение показателя ХЛ на фоне низкого содержания ТБК-продуктов, сывороточного железа, общей железосвязывающей способности организма.
- дефицит микроэлементов, коррелирующий со снижением индекса фагоцитоза, угнетением окислительной способности печени (медь, железо). Необходимо особо отметить, что железодефицит (постоянный спутник ожоговой болезни) является одной из причин хронического анемического синдрома, вызывает депрессию митохондриального и микросомального окисления, усугубляя состояние больного.
Очевидно, что при оценке статуса важно учесть все полученные показатели, чтобы определить уровень обменных процессов, метаболические ресурсы организма. Существующая тенденция считать гиперметаболизм постоянным синдромом у всех тяжелообожженных пациентов и, проводить соответствующую терапию, на наш взгляд, не имеет оснований. По нашим данным, это короткий период, быстро переходящий в стадию метаболического истощения, которая требует в большей степени заместительной терапии.
Как упоминалось выше, термин срочная адаптация подразумевает спад стрессовой реакции и восстановление утраченных функций систем и органов до исходного уровня. Этот процесс происходит постепенно: на клеточном уровне, органном, системном и организменном.
Суждение о том, что по выходу из шока больные достигают стадии срочной адаптации, т.к. возвращаются к норме некоторые гемодинамические показатели, на наш взгляд, неверно. Как известно по литературным данным, а также в результате наших исследований, повышенный стероидный фон, обеспечивающий наряду с многочисленными клеточными медиаторами запуск неспецифической реакции на стресс, наблюдается у больных еще длительное время, вплоть до подготовки ран к пластике. Затем наступает короткий переходный период — до закрытия ран — и, далее в течение месяцев и года больные находятся в состоянии длительной адаптации, отличительным признаком которой является гипертрофия доминирующих систем. В нашем случае, в первую очередь, это продолжающаяся интенсификация обменных процессов и гипертрофия соединительной ткани. Затем наступает период деадаптации.
Эти вопросы не являются чисто теоретическими: знание направленности метаболических изменений в организме позволит осуществить более тонкое их регулирование для достижения скорейшей стабилизации.
Например, в результате наших исследований мы определили ряд биохимических критериев срочной адаптации на системно-органном уровне, т.е. тот фон возврата к исходному метаболическому уровню, к которому стремится организм: умеренно повышенное или нормальное содержание стрессовых гормонов, но не их истощение; восстановление рутинных биохимических параметров; снижение катаболизма белка (экскреция азота АК увеличена не более, чем в 1.5-2 раза); умеренная гипераминоацидемия; нормализация в системе про-и антиоксидантов; относительное восполнение потерь микроэлементов; стабилизация иммуно-и коагулограмм.
По-видимому, больные с обширными ожогами полной адаптации не достигают никогда, поэтому их состояние неполной адаптации можно назвать маладаптацией.
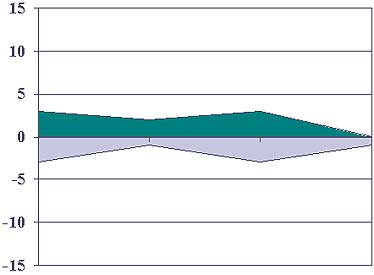
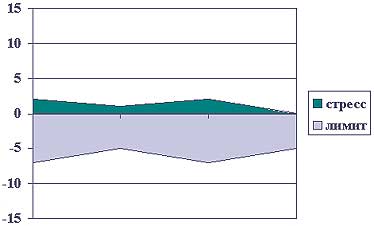
В процессе дальнейшего изучения стрессовой реакции мы определили каждый параметр как стресс-запускающий или стресс-лимитирующий, и стало очевидно, что больных по степени выраженности той или другой систем можно распределить на группы или варианты (рис 1). Мы установили три типа адаптограмм: гиперметаболический (гиперстресс), умеренно-компенсаторного гиперметаболизма (нормостресс) и гипометаболический (гипостресс).
Рис.1 Типы адаптограмм
Гиперметаболизм (гиперстресс)
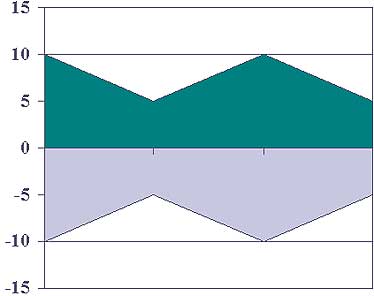
Принцип лечение -подавление
Умеренно-компенсаторный гиперметаболизм (нормостресс)
Гипометаболизм (гипостресс)
В основу этой классификации нами положен принцип взаимоотношения стресс-запускающих и стресс-лимитирующих систем. Стресс-запускающая система включает, как известно, мозговые и гипоталамические ядра, гипофиз-адреналовую и эффекторную симпатическую части. Стресс-лимитирующая представлена ГАМК-ергической, опиоидной, допамин и серотонинергической системами, на периферии-простагландинами, антиоксидантами, АТФ-системой и системой стрессовых протеинов Hsp-70.
По нашим данным при наиболее благоприятном, втором типе- нормострессе- наблюдается относительно равномерное напряжение этих систем: отклонение показателей от нормы не более, чем в 3-4 раза. При первом -гиперстрессе- наблюдается выраженное преобладание стресс-запускающих систем на фоне также выраженного угнетения стресс-лимитирующих: отклонение от нормы тех и других — в 8-10 раз. При неблагоприятном течении этот вариант быстро приводит к истощению и сепсису. Третий тип — гипостресс- характеризуется слабым стрессовым фоном и значительным белковоэнергетическим дефицитом, лежащим в основе стресс-лимитирующей системы. Этот вариант наблюдается у пожилых, с исходным преморбидом, а также в случае выхода из гиперстресса. Он также чреват развитием ПОН и сепсиса.
При изучении метаболического статуса больных (20 наблюдений), у которых в дальнейшем развились ПОН и сепсис, мы определили ряд прогностически неблагоприятных метаболических признаков протекания стрессовой реакции, а именно:
- быстрый спад гормонального фона (17 ОКС в большинстве случаев не определялись);
- выраженная, не поддающаяся коррекции гипопротеинемия (содержание общего белка менее 50 г/л);
- аналогичная «злокачественная» анемия (общий гемоглобин не более 70 г/л);
- стойкое железодефицитное состояние (не более 5 мкг/л);
- гипохолестеринемия и значительный дефицит HDL (не более 0,5);
- снижение окислительной способности печени (низкое содержание ТБК-продуктов, билирубина, гипо-и аферментемия);
- углубляющийся иммунодефицит и коагулопатия потребления.
Неблагоприятные вышеуказанные тенденции протекания стрессовой реакции, приводящие к развитию метаболического истощения, являются, на наш взгляд, следующей за SIRS стадией, предшествующей развитию сепсиса; а наличие всего комплекса признаков — метаболическим фоном сепсиса.
В связи с вышеизложенным, определение типа адаптограммы, т.е. изучение формы протекания стресс-реакции, комплексная оценка метаболического статуса пациента является крайне важной для выявления прогностически неблагоприятных тенденций и проведения своевременной профилактики срыва адаптации, а также, для изначального регулирования процесса. В случае выраженного гиперметаболизма основные усилия необходимо направлять на подавление: седация, антиоксиданты, ингибиторы протеолиза, интенсивная детоксикация. При компенсаторном гиперметаболизме основным принципом должно быть сохранение резервных возможностей больного, т.е. умеренная детоксикация, стимуляция, симптоматическое замещение. И, если имеется тенденция к гипометаболизму, то на первый план выступает заместительная терапия, метаболическая поддержка, стимуляция окислительных процессов.
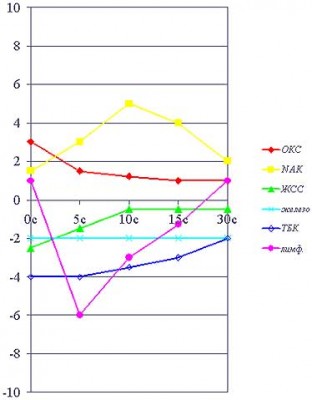
Например, больному Ш. (рис. 2) с ожогами пламенем IIIАБ-IV ст. 26% поверхности тела, термоингаляционной травмой — в острый период на фоне повышенного собственного уровня стероидов было применено дополнительное болюсное введение глюкокортикоидов, что привело к гиперстрессу (экскреция 17 ОКС и 17 КС возросла в 8-10 раз) и преждевременному выраженному метаболическому истощению. Уже при первом обследовании выявлено угнетение обменных процессов: показатели про- и антиоксидантной функции организма были снижены в 1.5-3.0 раза (ТБК-продукты, каталаза, HDL, ЖСС, спонтанная ХЛ). При этом рутинные биохимические, коагуологические и общеклинические параметры — в пределах нормы. Общее состояние больного стабильное тяжелое. Через неделю проявляются системные патохимические расстройства: гипопротеинемия (общий белок падает до 40.6, альбумин — до 23.4), анемия (гемоглобин — 88.0), гипокоагуляция (АЧТВ — 113.0, тромбиновое время — 110.0, фибриноген — 0.8, тромбоциты — 92.0, ПТИ — 30.0). Клинически состояние остается прежним, однако появляются эпизоды гипотонии и гипертермии. Усилено энтеральное и парентеральное питание, продолжается проведение комплексной детоксикационной терапии. Гипосостояние по адаптограмме наблюдается и следующую неделю. Следующий этап — истощение клеточных резервов: прогрессирует анемия (HB — 62.0, эритроциты — 2.0), развивается лимфопения (8.0-10.0), нарастает лейкоцитоз, появляются юные формы. Периодически отмечается нестабильность гемодинамики, тахиаритмия, гипертермия с ознобом. Экскреция стрессовых гормонов резко падает. Все это потребовало включения в заместительную терапию неоднократных гемотрансфузий и повторного длительного курса преднизолона. В результате значительных усилий удалось стабилизировать состояние больного и подготовить раны к пластике.
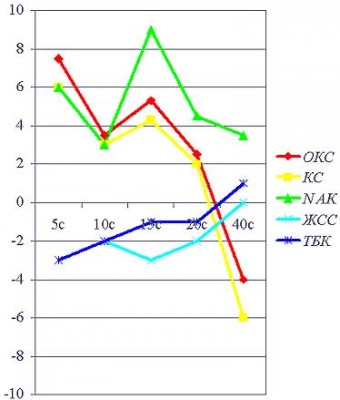
Рис.2 Адаптограмма больного С.
Адаптограмма больного Ш.
Следующий пример (рис. тот же) демонстрирует своевременную диагностику гипометаболического состояния и проведения соответствующих профилактических мер выраженного метаболического истощения. При поступлении у больного с ожогами пламенем IIIаб-IV степени 30% поверхности тела (IIIб-IVст.-20%) на фоне инсулинзависимого сахарного диабета, ожирения II ст. по адаптограмме диагносцирован нормостресс с тенденцией к гипо. Состояние пациента тяжелое, обусловленное токсемией. Гемодинамика стабильна, лабораторные показатели в допустимых пределах. При повторном обследовании отмечается преждевременный спад стрессовой реакции, железодефицитное состояние. Назначение поддерживающих доз преднизолона на две недели раньше общепринятого, дробных гемотрансфузий, а также железосодержащих препаратов на фоне раннего энтерального питания и комплексной детоксикационной терапиии определило стабильность состояния данного пациента. В острый период отмечался однократный подъем температуры до 39 град.С, содержание общего белка ни разу не опускалось ниже 60.0, а гемоглобина — 90.0, состояние гемостаза характеризовалось умеренной гиперкоагуляцией II степени. Больной своевременно и с минимальными затратами подготовлен к оперативному лечению, несмотря на наличие тяжелых ожогов и сопутствующей патологии.
Выводы
- Лечебно-диагностическую тактику, в том числе тяжелой термической травмы, необходимо планировать с позиций не только патологии, но и компенсации нарушенных функций.
- Тщательное изучение характера протекания системного ответа на стресс при термической травме способствует своевременному выявлению неблагоприятных тенденций метаболического истощения. С этой целью целесообразна комплексная оценка метаболического статуса пациента.
- Метаболическое истощение, на наш взгляд, является следующей за SIRS стадией, предшествующей развитию сепсиса.
Литература
- Алексеев А.А., Т.А. Ушакова, М.Г. Крутиков, Л.В. Елагина, В.А. Лавров//Сепсис как срыв адаптивных реакций организма на ожоговую травму//Матер. Межд. конф. «Актуальные проблемы термической травмы», С-Петерб., 2002, с.114-116.
- Алексеев А.А., Т.А. Ушакова, В.А. Лавров, М.Г. Крутиков//Изучение адаптивных реакций организма на ожоговую травму и раннее хирургическое лечение//Матер. XX съезда хир.Украины, т2, Тернополь,2002,543-544.
- Волчегорский И.А., Долгушин И.И., Колесников Д.Л., Цейликман В.О. //Экспериментальное моделирование и лабораторная оценка адаптивных реакций организма// Челябинск, 2000г, 168с.
- Заец Т.Л. //Нарушения белкового обмена и некоторых звеньев его регуляции при термических ожогах//дисс. док. мед. наук, Москва, 1969.
- Николас А. Майер//Использование питательных веществ в процессе заживления ран//Анес. и реан., 1996, 5, 29-37.
- Онищенко Н.А., В.А. Сускова, А.Б. Цыпин, А.М. Маремшанов, Л.П. Ермакова//Полиорганная недостаточность как проявление иммунной дисрегуляции репаративных процессов в органах при критических состояниях //Анест. и реан., 2001, 3, 54-58.
- Петров В.Н.//Физиология и патология обмена железа//Л., Наука, 1982, 224с.
- Саркисов Д.С. //Структурные основы адаптации и компенсации нарушенных функций// М., Медицина, 1987, 448с.
- Селье Г.//Очерки об адаптационном синдроме//М., Медгиз, 1960, 254с.
- Сергеев П.В. //Стероидные гормоны//, М., 1984.
- Слепушкин В.Д., Васильев С.В. //Оптимизация метаболизма у больных в критических состояниях// Вест. Рос. АМН, 1997, N10, 59-61.
- Тигранян Р.А.//Гормонально-метаболический статус организма при экстремальных воздействиях//М., Наука, 1990.
- Ушакова Т.А., В.А. Лавров, Л.В. Елагина//Метаболический дисбаланс как критерий степени тяжести обожженных//Сб.науч.тр.конф. «Комбустиология на рубеже веков», Голицыно, 2000,с73.
- Ушакова Т.А., В.А. Лавров, Л.В. Елагина, С.В. Попов//Типы метаболического ответа на термическую травму//Сб.тр. «Успехи теорет. и практ. медицины», Москва, 2001, с56.
- Alexeev A.A., T.A. Ushakova, V.A. Lavrov, L.V. Elagina, S.V. Popov// The Investigation of adaptive reactions in severely burned patients// EBA Posters book (9-th Congress of the European Burns Association), 2002, p80.
- Ambrosi B., Re T., Passini E. et al //J. Endocrinol.Invest.-1996.-Vol.19, N4.-P.204-209.
- Kelestimur F., Sahin Y., Ayata D., Tutus A.//Clin.Endocrinol.-1996.-Vol.45, N4 -P381-384.
- Lapshin A.V., Manukhina E.B., Meerson F.Z. et. al //Hyp. Med. J. 1995. v3.N1-P3-6.
- Meerson, F.Z. //Concept of Long-Term Adaptation//Delo, Moskow.
- Ross R, Miell J, Freeman E, et al //Critically ill patients have high basal growth hormone levels with attenuated oscillatory activity associated with low levels of insulin-like growth factor-1// Clin Endocrinol 1991; 35, 47-54.
- Schroeder S, Wishers M, Klingmuller D, Hofer M et al //The hypothalamic-pituitary-adrenal axis of patients with severe sepsis: altered response to corticotropin-releasing hormone//Crit.Care Med.2001, Feb; 29(2): 450-1.
- Van den Berghe G. de Zegher F, Schetz M, Verwaest C, Ferdinande P, Lauwers P.//Dehydroepiandrosterone sulphate in criticall illness: effect of dopamine//Clin.Endocrinol 1995; 43: 451-463.
- Wilmore, D.W., C.W. Goodwin, L.H. Aulick // Catabolic illness: Strategies for enhancing recovery// 1991; N. Engl. J.Med 325(10): 695-702.
- Wilmore, D.W., C.W. Goodwin, L.H. Aulick // Homeostasis: Bodily changes in trauma and surgery// Pp 55-67 in Textbook of Surgery, 15 th ed., D.C. Sabiston.
- Yu. Malyshev and E.B. Manukhina //Stress, Adaptation, and Nitric Oxide// Journal Contents Biokhimiya Home page N7.
Designed by Сайт на Заказ