
ОБЪЕДИНЕНИЕ КОМБУСТИОЛОГОВ
«МИР БЕЗ ОЖОГОВ»
Ожоговый шок: инвазивный мониторинг
Виноградов В.Л.
Лавров В.А.
г.Москва, Институт хирургии им. А.В.Вишневского РАМН.
Основная функция сердечно-сосудистой системы заключается в снабжении тканей питательными веществами и кислородом. Тяжелая ожоговая травма может серьезно изменить метаболические потребности организма, а также работу всех звеньев системы доставки кислорода, к которым относятся сердечный выброс, содержание кислорода в артериальной крови и утилизация кислорода. По данным многих авторов смертность от ожогового шока обусловлена несоответствием количества поступающего кислорода и метаболическими запросами организма. Поэтому становится понятно, что один лишь контроль таких параметров гемодинамики, как число сердечных сокращений, измерение артериального давления непрямым методом, центральное венозное давление и измерение газового состава в капиллярной крови недостаточен для решения вопроса об адекватности проводимой терапии. Считается, что у пострадавших с глубокими и обширными ожогами общей площадью более 45% (даже без наличия предшествующей сердечной патологии) должен проводиться инвазивный мониторинг центральной гемодинамики при помощи катетеризации периферической артерии и установки флотирующего катетера типа Swan-Ganz в легочную артерию с последующим контролем газового состава артериальной и смешанной венозной крови.
Измерение давления в периферической артерии прямым методом (IBP — Invasive Blood Pressure)
В медицине существует много методик, которые недостаточно точны, но очень популярны. К таковым относится и всем хорошо известный метод измерения артериального давления с помощью манжеты (NIBP — NonInvasive Blood Pressure).
Причины ошибок:
- надувание и спускание манжетки увеличивает объем крови и давление в области измерения;
- у больных пожилого возраста, страдающих гипертонической болезнью, при измерении артериального давления непрямым методом, полученные результаты превышают истинные значения по крайней мере на 10%. Ложное повышение диастолического давления часто отмечается у лиц с ожирением, особенно, если манжетка наложена неплотно. Наоборот, наложение манжеты с захлестом у астенизированных больных нередко занижает истинные значения.
При нестабильной гемодинамике непрямой метод измерения артериального давления всегда дает ложные результаты. В некоторых ситуациях отклонения от истинных значений в измерении систолического давления могут достигать огромных величин (30-60 мм.рт.ст).
Риск получения ошибочных результатов у пациентов с низким сердечным выбросом является основной причиной того, что использование NIBP нежелательно у больных, находящихся в критическом состояниях.
Стандартная методика измерения артериального давления у больных, находящихся в критическом состоянии, заключается в катетеризации лучевой или бедренной артерии. Хотя систолическая и диастолическая составляющая разнятся по мере продвижения пульсовой волны от проксимального отдела аорты к ее разветвлениям (рисунок 1), величина среднего артериального давления (AДср, MAP) практически не меняется и не зависит от погрешностей измерения. Современные мониторы самостоятельно рассчитывают MAP и постоянно выводят его значение на экран. Наиболее распространенные места катетеризации артериального русла у взрослых — лучевая и бедренная артерия.
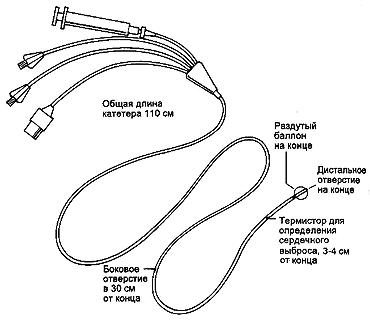
Рис.1
Пульсовые волны артериального давления в различных отделах артериальной системы.
Помимо измерения артериального давления, канюляция периферической артерии дает возможность следить за кислотно-основным состоянием и газовым составом артериальной крови без излишней травматизации больного.
Частота осложнений при катетеризации как бедренной артерии, так и лучевой сильно не отличаются и составляют 7-10%. Однако ишемические повреждения пальцев конечностей не превышают 3%, а стойкие нарушения наблюдаются весьма редко. Частота инфекционных осложнений такая же, как и при других артериальных и венозных катетеризациях, и составляет 1-3%.
Катетеризация лёгочной артерии
Для катететеризации легочной артерии используют флотационно-балонный катетер типа Swan-Ganz (рисунок 2).
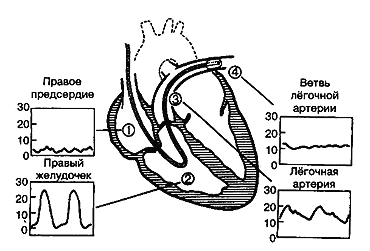
Рис.2
Флотационный катетер Swan-Ganz для катетеризации легочной артерии.
Принцип установки плавающего катетера напоминает движение лодки. Специальный баллончик на конце катетера раздувают воздухом, и по току крови он проводит катетер в верхнюю полую вену. Далее катетер через правый отдел сердца попадает в лёгочную артерию (рисунок 3).

Рис.3
Изменение формы кривой давления по мере продвижения катетера из правово предсердия в легочную артерию.
Гемодинамический профиль
При катетеризации легочной артерии и периферической артерии можно получить ряд показателей как регистрируемых, так и расчетных, которые объединяют общим термином «гемодинамический профиль». Он включает в себя параметры гемодинамики, которые позволяют достаточно полно оценить состояние кровообращения пациента прямо у его постели.
Регистрируемые показатели кровообращения измеряемые прямым методом
Помимо прямого измерения артериального давления и давления в легочной артерии при помощи катетера Swan-Ganz измеряют следующие показатели (таблица 1).
- Центральное венозное давление (ЦВД, CVP) — давление в правом предсердии. Давление в правом предсердии соответствует конечному диастолическому давлению в правом желудочке при условии отсутствия обструкции между предсердием и желудочком.
- Давление заклинивания в лёгочных капиллярах (ДЗЛК, PCWP) — давление в дистальной ветви лёгочной артерии при раздутом баллончике. Это давление считается равным давлению в левом предсердии или конечному диастолическому давлению в левом желудочке.
- Сердечный выброс (МОС, CO) измеряют с помощью термистора, который находится рядом с дистальным концом катетера. Сердечный выброс определяют по скорости изменения температуры крови в легочной артерии после болюсного введения раствора более низкой температуры, чем кровь. Этот способ получил название «метод терморазведения, или термодилюции».
- Насыщение кислородом смешанной венозной (SvO2) крови измеряют при катетеризации лeгочной артерии либо in vivo с помощью специального катетера, либо in vitro в порции крови, взятой из лёгочной артерии через дистальное отверстие катетера. Насыщение кислородом смешанной венозной крови используется как показатель экстракции кислорода тканями из крови.
Производные параметры
При помощи расчетов число показателей центральной гемодинамики и кислородно-транспортной функции крови значительно увеличивается Эти показатели представлены в таблице2. С целью нивелирования влияния индивидуальных антропометрических значений каждый расчетный показатель можно индексировать относительно площади поверхности тела (в квадратных метрах).
- Сердечный выброс (МОС, CО) — определяет насосную функцию сердца и показывает какое количество крови сердце перекачивает за 1 минуту.
- Ударный объем (УО, SV) — объем крови, выбрасываемый сердцем во время каждой систолы.
- Ударная работа левого желудочка (УРЛЖ, LVSW) характеризует работу левого желудочка при выбросе крови в аорту за 1 сокращение.
- Ударная работа правого желудочка (УРПЖ, RVSW) характеризует работу правого желудочка при выбросе крови в аорту за 1 сокращение.
- Общее периферическое сопротивление сосудов (ОПСС, SVR). Этот показатель характеризует общее сопротивление всей сосудистой системы выбрасываемому сердцем потоку крови.
- Сопротивление лёгочных сосудов (СЛС, PVR) характеризует сопротивление лёгочных сосудов (от лёгочной артерии до левого предсердия).
- Доставка кислорода (кислородный поток) (КП, DO2) отражает количество кислорода, доставляемого к капиллярам за 1 мин.
- Потребление кислорода (ПO2, VO2) — количество кислорода, поглощаемого тканями в течение 1 мин.
- Коэффициент утилизации (экстракции) кислорода (O2 Ext) отражает долю поглощаемого тканями кислорода из капиллярного русла или баланс между доставкой и потреблением кислорода.
Осложнения
Катетеризация лёгочной артерии невозможна без побочных эффектов, но лишь некото-рые из них опасны для жизни. Многие из этих осложнений неспецифичны и наблюдаются при использовании практически всех типов внутрисосудистых катетеров. Однако некоторые осложнения специфичны только для катетеризации лёгочной артерии.
- Желудочковые аритмии встречаются более чем у 50% больных при продвижении катетера через правый отдел сердца. Обычно эти аритмии гемодинамически незначимы и проходят при удалении катетера.
- Разрыв легочной артерии — очень редкое осложнение. 0бычно это осложнение проявляется остро возникающим кровохарканьем и часто заканчивается летальным исходом.
Структурный подход к диагностике и тактике ведения шока
С целью диагностики любого вида шока и выбора тактики в его лечении можно предложить структурный подход, сформулированный Е Норманом и МД Фримен, который основывается на анализе всего 6 показателей и осуществляется в 2 этапа. Этот подход не определяет шок как артериальную гипотензию или гипоперфузию, скорее он представляет его как состояние неадекватной оксигенации тканей. Конечная цель такого подхода — добиться соответствия между доставкой кислорода к тканям и уровнем метаболизма в них, поэтому он базируется на анализе ряда показателей, которые можно представить себе в виде 2-х групп:
- Давление/кровоток:
- давление заклинивания в легочных капиллярах (PСWP).
- сердечный выброс (CO).
- общее периферическое сопротивление (SVP).
- Транспорт кислорода:
- Доставка кислорода (DO2).
- Потребление кислорода (VO2).
- Состояние кислотно-основного баланса (КОС).
I этап: малые гемодинамические профили
На этом этапе используют комплекс параметров «давление/кровоток» с целью определения и коррекции ведущих нарушений гемодинамики. Цель этого этапа — восстановить артериальное давление и кровоток (если возможно) и установить причину патологического процесса. Для упрощения считается, что каждый фактор из этой группы играет ведущую роль в одном из основных видов шока:
- PCWP — при гиповолемическом шоке;
- CO — при кардиогенном (острая сердечная недостаточность);
- SVP — при анафилактическом.
Взаимоотношения PCWP, CO и SVR при указанных разновидностях шока могут быть представлены так называемыми малыми гемодинамическими профилями, способствующие определению индивидуального подхода в каждом конкретном случае.
Гиповолемический шок
При нем первостепенное значение имеет снижение наполнения желудочков, которое приводит к уменьшению СО (в соответствии с уравнением Фика), что в свою очередь вызывает вазоконстрикцию, которая проявляется в увеличении SVR. Поэтому «формула» гиповолемического шока будет иметь вид:
vPCWP/vCO/^SVR
Кардиогенный шок
В этом случае ведущим фактором является острая сердечная недостаточность со снижением CO, с последующим застоем в легочном круге кровообращения (высокий SVR) и периферической вазоконстрикцией (высокий SVR). «Формула» кардиогенного шока имеет следующий вид:
^PCWP/vCO/^SVR
Анафилактический шок (септический)
Особенностью этого вида шока является резкое падение тонуса артерий (низкое SVR) и в различной степени вен (низкое PCWP). Сердечный выброс, особенно в начальной фазе, обычно высок, но его величина может варьировать. «Формула» анафилактического шока имеет следующий вид:
vPCWP/^CO/vSVR
Сложные сочетания гемодинамических показателей при ожоговом шоке
Как отмечалось в предыдущей лекции ожоговому шоку характерен ряд присущих только для него особенностей, хотя его и можно отнести к разновидности гиповолемического шока. Наиболее характерными из них являются:
- длительность течения;
- массивные сдвиги в водных пространствах организма;
- выраженная интоксикация;
- повышение проницаемости стенок капилляров;
- выраженное нарушение кислотно-основного состояния.
В первые 12-24 часа проявления ожогового шока в большей степени будут соответствовать классическому гиповолемическому шоку, т.е. его «формула» будет иметь вид:
vPCWP/vCO/^SVR
Однако не следует забывать, что снижение сердечного выброса в этот период может быть обусловлено не только гиповолемией, но и уменьшением сократительной функции миокарда, которую отчасти можно объяснить выбросом миокардиодепрессивных факторов. Поэтому, если в результате инфузионной терапии удалось стабилизировать PCWP на приемлемых цифрах, но сердечный выброс остается на неудовлетворительном уровне, в схему терапии шока следует включить кардиотонические средства, т.к. дальнейшее увеличение темпа инфузии может вызвать легочную гипертензию и отек легких.
В период со 2-го по 5-й день развивается гипердинамическая стадия кровообращенияв, которая соответствует развитию острой ожоговой токсимии: повышается сердечный выброс и в значительной степени снижается общее периферическое сопротивление сосудов. При этом происходит развитие максимального отека тканей В этот период малый гемодинамический профиль будет в большей степени соответствовать анафилактическому шоку:
vPCWP/^CO/vSVR
Величина PCWP может быть нормальной, если венозный тонус не изменен или повышена жесткость желудочка.
В целом же сочетание основных показателей гемодинамики в период ожогового шока может быть различным. Это определяется как сопутствующей патологией пострадавшего (например, сердечная недостаточность), так и отягощающие факторы самой травмы (например, термоингаляционное поражение). Не следует сбрасывать со счетов и ятрогенные факторы. Существует 27 малых гемодинамических профилей, но каждый можно истолковать на основе 3 главных «формул». Для этого следует определить ведущее нарушение кровообращения.
Например «формула» имеет вид:
vPCWP/vCO/норма — SVR
В данном случае гемодинамические характеристики напоминают гиповолемический шок, за исключением нормальной величины общего периферического сопротивления. Такое состояние можно охарактеризовать как гиповолемию с низким тонусом сосудов. Поэтому терапия должна включать в себя как введение жидкости, так и применение средств, повышающих SVR (например, дофамин).
Коррекция нарушений гемодинамики требует применение соответствующих лечебных мероприятий. В нашу задачу не входит подробный анализ методов лечения шока, поэтому мы ограничимся схематическим отражением принципов коррекции нарушений гемодинамики при шоковых состояниях.
|
Состояние |
Терапия |
| Низкое или нормальное PCWP | Инфузионная терапия |
| Низкий CO | |
| при высоком SVR | Добутамин |
| нормальное SVR | Дофамин |
| Низкий SVR | |
| сниженный или нормальный CO | альфа, бета-Агонисты |
| высокий CO | альфа-Агонисты |
Наличие у дофамина в средних дозах кардиотонической активности, сочетающейся с влиянием на сопротивление регионарных сосудов, а в высоких — выраженных альфа-адреномиметических свойств, делает его весьма ценным противошоковым препаратом. В некоторых случаях дофамин можно заменить норадреналином если возникает необходимость быстро получить сосудосуживающий эффект (например, при септических состояниях) или повысить артериальное давление. Следует помнить, что при гиповолемическом шоке с резким падением давления норадреналин применять нельзя, т.к. это приводит к резкому ухудшению кровоснабжения тканей.
II этап — оксигенация тканей
Шок может быть определен как состояние, при котором потребление кислорода тканями неадекватно их потребностям для аэробного метаболизма. Гемодинамические показатели не могут указать на степень ишемии органов и тканей. С этой целью используют показатели группы «транспорт кислорода».
Наиболее важный из них — показатель «потребление кислорода» (VO2), который определяет поглощение (захват) кислорода из микроциркуляторного русла, но не отражает его расход в метаболических процессах. Низкие значение VO2 (алкалоз, гипоксемия, высокий тканевой шунт) могут указывать на неадекватное поглощение кислорода тканями, если только уровень метаболизма в них не снижен. Однако нормальное или высокое значение VO2 еще не гарантирует достаточного обеспечения тканей кислородом. Ишемия тканей будет развиваться, если уровень метаболизма в них превышает потребление кислорода, невзирая на величину VO2. В этих случаях у пострадавших развивается метаболический ацидоз за счет накопления в тканях молочной кислоты в результате анаэробного метаболизма. Следовательно показатели КОС или непосредственное определение уровня молочной кислоты могут использоваться для оценки баланса потребления тканями кислорода и его расходования в метаболических процессах и одновременно служить критериями адекватности проводимого лечения. Подход, применяемый на II этапе, позволяет оценить оксигенацию тканей и выбрать дальнейшее направление терапии, т.к. нормализация только гемодинамических показателей еще не говорит о выходе больного из шока. Так же, как и нормальные цифры VO2, но сохраняющиеся нарушения КОС, не являются показанием к прекращению противошоковых мероприятий.
Таким образом, для всех тяжелообожженных, находящихся в ожоговом шоке, рекомендуется мониторирование центральной гемодинамики и кислородно-транспортной функции крови. Ориентация на такие показатели как сердечный выброс (СО), давление заклинивания легочной артерии (PCWP), общее периферическое сопротивлению сосудов (SVR), потребление кислорода (VO2) способствует адекватному проведению инфузионной терапии, своевременному подключению инотропных препаратов, правильной оценке тканевой перфузии, доставке и потреблению тканями кислорода, тем самым предупреждает повреждение и гибель еще жизнеспособных тканей ожоговой раны, что в конечном итоге определяет прогноз для наиболее тежело обожженных пациентов.
Заключение
Проблема лечения ожогового шока конечно несравненно гораздо шире того круга вопросов, которые были затронуты в нашей лекции. На показатели гемодинамики и кислородно-транспортной функции крови влияет масса, не затронутых нами, факторов. Это нарушение реологических свойств крови, белкового баланса, поражение паренхимы легких, инфекционные процессы и т.д. Инвазивный мониторинг не является рутинным методом, применяемым у тяжелообожженных. Однако более широкое внедрение его в клиническую практику будет способствовать повышению эффективности противошоковых мероприятий, проводимых не только в специализированных ожоговых центрах, но и отделениях интенсивной терапии обычных больниц.
Рекомендуемая литература
Гриппи МА. Патофизиология легких. М, Бином, 1997.
Интенсивная терапия. (под ред. Марино П).М, ГЭОТАР Медицина, 1998.
Ожоги у детей (под ред.Карваял ХФ, Паркс ДХ). М, Медицина, 1990
Рябов ГА Гипоксия критических состояний. М, Медицина, 1988.
Шок. (под ред. Риккер Г). М, Медицина, 1987.
Thys DM, Reich DL. Invasive cardiovascular monitoring (In: Monitoring in Anesthesia, edited by Saidman LJ, Smith NT — 3rd ed). Butterworth-Heinemann,1993.
|
Таблица 1 |
||||
|
Параметр |
Принятые сокращения |
единицы |
||
| в отечественной литературе | международное | |||
| Частота сердечных сокращений | ЧСС | HR | уд/мин | |
| Среднее артериальное давление | АДср, САД | MAP | мм.рт.ст | |
| Центральное венозное давление | ЦВД | CVP | мм.рт.ст | |
| Среднее давление в легочной артерии | ДЛАср | MPA | мм.рт.ст | |
| Давление «заклинивания» в легочной артерии | Рзакл, ДЗЛК | PCWP | мм.рт.ст | |
| Сердечный выброс (минутный объем сердца) | МОС, МОК, СВ | СО | л/мин | |
| Парциальное давления кислорода и углекислого газа в артерии. | PaO2, PaСO2 | PaO2, PaO2 | мм.рт.ст | |
| Парциальное давления кислорода и углекислого газа в смешанной венозной крови. | PvO2, PvСO2 | PvO2, PvCO2 | мм.рт.ст | |
| Насыщение артериальной и смешанной венозной крови кислородом | SaO2, SvO2 | SaO2, SvO2 | % | |
|
Таблица 2 |
|||||
|
Показатель |
Принятые сокращения |
|
единицы |
||
| в отечественной литературе | междуна- родное |
||||
| Площадь поверхности тела | ПТ | BSA | Рост0,725*Вес0,425*0,007184 | м2 | |
| Ударный объем сердца | УО | SV | CO/HR | мл*уд-1 | |
| Общее периферическое сосудистое сопротивление | ОПСС, ОПС | SVR | (AP-CVP)/CO*79.9 | дин*с*см-5 | |
| Легочное сосудистое сопротивление | ЛСС, ОЛС | PVR | (MAP-PCWP)/CO*79.9 | дин*с*см-5 | |
| Ударная работа левого желудочка | УРЛЖ, РЛЖ | LVSW | (MAP-PCWP)*SV*0.0136 | г*мин*уд-1 | |
| Ударная работа правого желудочка | УРПЖ, РЛЖ | RVSW | (MPA-CVP)*SV*0.0136 | г*мин*уд-1 | |
| Содержание кислорода в артериальной крови | CaO2 | CaO2 | 1.34*Hb*SaO2/100+PaO2*0.0031 | мл*дл-1 | |
| Содержание кислорода в смешанной венозной крови | CvO2 | CvO2 | 1.34*Hb*SvO2/100+PvO2*0.0031 | мл*дл-1 | |
| Артерио-венозная разница по кислороду | AvDO2 | AvDO2 | CaO2 — CvO2 | мл*дл-1 | |
| Доставка кислорода (кислородный поток) | КП | DO2 | CaO2*CO*10 | мл*мин-1 | |
| Потребление кислорода | ПО2 | VO2 | AvDO2*CO*10 | мл*мин-1 | |
| Экстракция кислорода (коэффициент утилизации кислорода) | КУО2 | O2ex | AvDO2/ CaO2 | доли или % | |
| Пол | Ж-13,7%, М — 86,3% | - |
| Возраст | 34,6+2,3 г. | - |
| Срок от тр. До пост. В спец. стационар | 12,5+2,6 дня | 10,5+2,4 дня |
| Койкодень | 77,4+2,7 дня | 97,5+ 3,4 дня |
| Общая площадь поражения | 40,7+1,8% | - |
| IIIБ -IVст. | 23,7+1,2% | - |
| Индукс Франка | 89+3,4 ед | - |
| ТИТ | 24,13% | - |
| ТКАФ от момента травмы | 36,5+2,1 дня | |
| ТКАФ от момента поступления в спец стац. | 24,1+1,4 дня | |
| КАДП с ТКАФ от момента травмы | 38,6+2,2 дня | 28,6+ 3,9 |
| КАДП с ТКАФ от момента поступления | 27,5+1,5 дня | 25,+ 2,5 |
| Площадь трансплантируемых клеток | 3915+201,6 см2 от 2550 до 5590см2 | |
| Эпителизация ячеек 1:6 | 11,96+0,2 дня | 22,4+ 0,3 |
| Эпителизация ячеек 1:4 | 7,36+0,2 дня | 11,7+ 0,2 |
| Эпителизация ячеек 1:8 | 15,36+0,2 дня | 29,1+0,4 |
| Осложнения при поступлении | 100% | |
| Сочетание осложнений | 75% | |
| Пневмония | 48,2% | |
| ЖКТ | 17,2% | |
| Истощение | 31% | |
| Другие | 3,6% | |
| Смертность | 3,2% | 14,7% |
| Закрытие ран от поступления | 27,5+1,5 дня | 54,2+3,1 |
| Эпителизация всех ран | 40,1+2,1 | 64,3+ 2,3 дня |
| Неприживление лоскута | 21,8% | 48,2% |
| Количество операций | 1,2+0,1 | 3,1+0,1 |